BioNTech провела первую фазу испытаний мРНК-вакцины против рака молочной железы
МЕНЮ
Главная страница
Поиск
Регистрация на сайте
Помощь проекту
Архив новостей
ТЕМЫ
Новости ИИ
Городские сумасшедшие
ИИ в медицине
ИИ проекты
Искусственные нейросети
Искусственный интеллект
Слежка за людьми
Угроза ИИ
ИИ теория
Компьютерные науки
Машинное обуч. (Ошибки)
Машинное обучение
Машинный перевод
Нейронные сети начинающим
Психология ИИ
Реализация ИИ
Реализация нейросетей
Создание беспилотных авто
Трезво про ИИ
Философия ИИ
Генетические алгоритмы
Капсульные нейросети
Основы нейронных сетей
Промпты. Генеративные запросы
Распознавание лиц
Распознавание образов
Распознавание речи
Творчество ИИ
Техническое зрение
Чат-боты
Авторизация
2026-04-10 11:38

Немецкая компания BioNTech сообщила о результатах наблюдений за 14 пациентками с трижды негативным раком молочной железы, получившими персонализированные мРНК-вакцины. Медианная продолжительность наблюдений составила пять лет. В настоящее время десять пациенток живут без рецидива, одна скончалась по неустановленной причине через 15 месяцев после вакцинации, и еще три умерли после рецидива. У многих участниц высокий уровень Т-клеток, активированных вакциной, сохранился на протяжении нескольких лет.
Компания BioNTech (Германия), известная разработкой вакцины против COVID-19, сообщает о результатах фазы I клинического исследования вакцины против рака молочной железы (РМЖ). В исследовании участвовало четырнадцать человек с хирургически удаленной трижды негативной опухолью молочной железы на ранней стадии. Десять пациенток в настоящее время живут без рецидива.
Трижды негативный рак молочной железы (ТНРМЖ) не имеет трех наиболее распространенных мишеней для лекарственной терапии — рецепторов эстрогена и прогестерона, а также рецептора эпидермального фактора роста второго типа (HER2), и не реагирует на стандартные методы лечения, блокирующие эти рецепторы. При этом ТНРМЖ составляет около 15% всех случаев рака молочной железы и чаще поражает молодых женщин. Он также более агрессивен, чем другие виды РМЖ, и имеет худший прогноз. На ранних стадиях хирургическая операция в сочетании с химиотерапией, лучевой терапией или иммунотерапией устраняет детектируемые опухоли, однако существует высокий риск рецидива и метастазирования в другие органы. Вероятность рецидива достигает пика в течение трех лет после постановки диагноза.
В качестве стратегий уничтожения остаточных опухолевых клеток рассматриваются персонализированные противоопухолевые вакцины. Опухолевые клетки накапливают мутации и экспрессируют измененные белки, называемые неоантигенами. Иммунная система может их атаковать, но эффективность распознавания и иммунного ответа обычно недостаточна для полного уничтожения.
Предполагается, что противораковое дейстие иммунной системы могут усилить персонализированные вакцины, которые содержат матричные РНК, кодирующие неоантигены — потенциальные мишени иммунного ответа. Противоопухолевые вакцины BioNTech содержат РНК не в липидных наночастицах, как в случае мРНК-вакцины против коронавируса, а в липоплексах — структурах, где мРНК находятся между липидными бислоями. Вакцина вводится внутривенно и достигает лимфоидных органов. Там она поглощается дендритными клетками которые экспрессируют неоантигены, презентируют их на своей поверхности и обучают Т-клетки их распознавать.
В исследовании, проведенном компанией BioNTech, оценивались осуществимость терапии мРНК-вакцинами, ее безопасность и механизм действия (характеристики иммунного ответа). Клиническая польза на этом этапе не была предметом исследования.
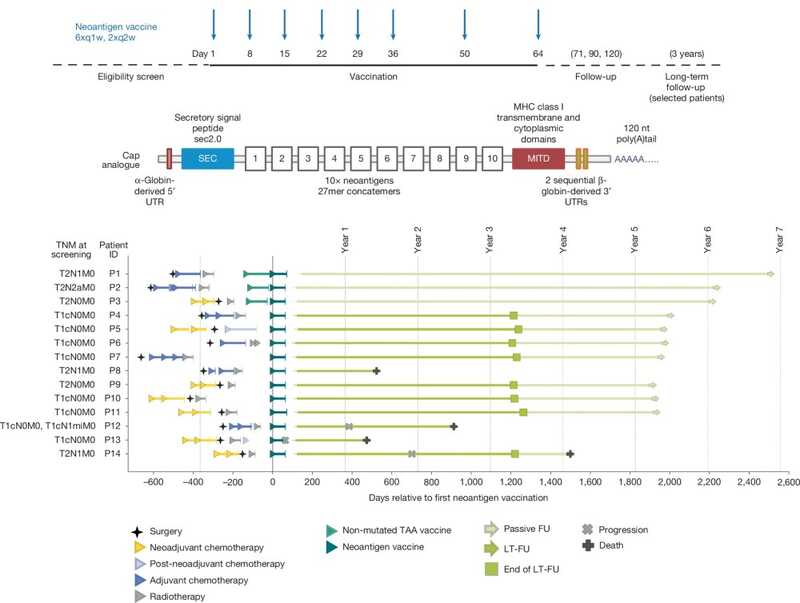
Сначала исследователи секвенировали опухолевые и здоровые клетки от 14 женщин с ранней стадией ТНРМЖ после хирургического удаления опухоли. (У пяти из них были обнаружены также метастазы в близлежащих лимфоузлах.) С помощью специальных алгоритмов провели отбор мутаций, генерирующих неоантигены. Для каждой участницы была изготовлена персонализированная мРНК-вакцина; все производственные циклы прошли в течение 2019 года. Среднее время производства вакцины, определяемое как период от получения образца до готовности продукта, составило 69 дней (от 34 до 125 дней). При этом авторы отмечают, что основная цель заключалась не в оптимизации времени производства, а в надежности действия.
Две молекулы мРНК в составе вакцины кодировали в общей сложности до 20 неоантигенов. Однонуклеотидные варианты (SNV), приводящие к замене аминокислоты, были представлены 27-мерными пептидами с измененной аминокислотой в центре; вставки или делеции, вызывающие сдвиг рамки считывания, — последовательностями от измененной аминокислоты до следующего стоп-кодона. Для усиления презентации на дендритных клетках последовательность неоантигенов была фланкирована секреторным сигнальным пептидом (SEC) и транспортным сигналом MHC I (MHC class I trafficking domain, MITD). Чтобы усилить трансляцию мРНК в презентирующей клетке, в ней были оптимизированы кэп, 5'- и 3'-нетранслируемые области (UTR) и конструкция поли(А)-хвоста. Добавим, что мРНК не содержала модифицированного уридина, в отличие от вакцин против респираторных вирусов. Не модифицированная таким образом РНК. как известно, обладает более сильными иммуногенными свойствами.
Все участницы получили восемь доз неоантигенной вакцины, а трех из них перед этим также иммунизировали немутантными антигенами, ассоциированными с опухолью (TAA, tumour-associated self-antigens).
Нежелательные эффекты, связанные с вакцинацией, ограничивались в основном временными гриппоподобными симптомами. По состоянию на февраль 2025 года у десяти человек за время наблюдения (медианная продолжительность пять лет) не было рецидива. Четыре участницы умерли, в трех случаях был рецидив, еще одна женщина скончалась через год и три месяца после введения последней дозы вакцины по неустановленной причине.
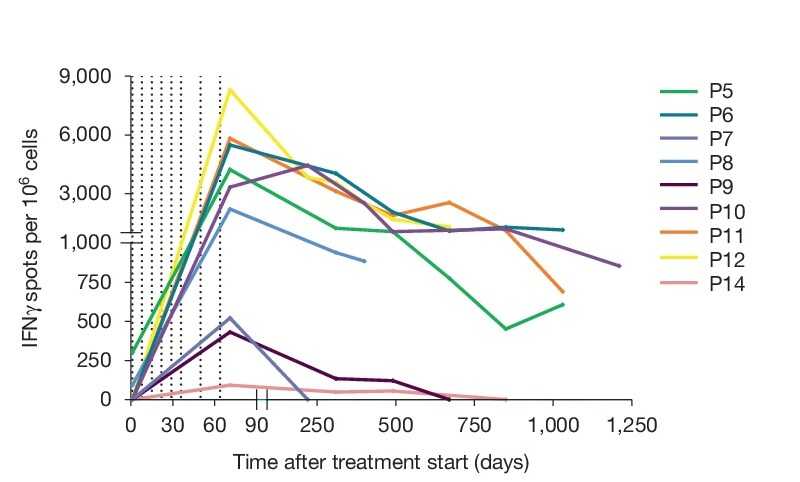
У всех участниц развился выраженный Т-клеточный ответ, причем у всех, кроме одной, наблюдался Т-клеточный ответ против множества неоантигенов. Для девяти человек были доступны данные по долгосрочной персистенции Т-клеток против неоантигенов (реагирующих на их присутствие экспрессией интерферона гамма, которую можно детектировать в тесте ELISpot). У шести уровень Т-клеток оставался высоким на протяжении нескольких лет, в том числе у умершей по неизвестной причине. Еще у трех, включая двух умерших после рецидива, реактивные Т-клетки со временем исчезли.
Персистирующие Т-клетки, как показали авторы, по большей части превратились в один из двух подтипов: эффекторные клетки, способные атаковать опухолевые клетки опухоли, или долгоживущие клетки памяти, обеспечивающие длительный иммунный надзор.
Авторы работы подробно исследовали три случая рецидива, чтобы определить их причины. В одном случае наблюдалась лишь слабая реакция на вакцину. В другом опухолевые клетки перестали экспрессировать молекулы главного комплекса гистосовместимости (MHC) класса I, соответственно, нарушилась презентация антигенов, и они стали «невидимыми» для Т-клеток, уклонившись таким образом от иммунного ответа. В третьем случае рецидивирующая опухоль генетически отличалась от исходной опухоли и не содержала неоантигенов, входящих в состав вакцины.
У одной из пациенток с безрецидивным периодом более шести лет удалось детально проанализировать Т-клеточные ответы, индуцированных вакциной. Показали, в частности, наличиет ответов против 10 мутаций, на которые была направлена вакцина, в том числе на восемь из них они были достаточно сильными. Неоантиген-специфические CD8 + Т-клетки сохранялись у нее на протяжении шести лет.
Таким образом, персонализированная мРНК-вакцинация безопасна и вызывает сильный и продолжительный иммунный ответ. В будущем необходимы более масштабные рандомизированные исследования, чтобы выяснить, улучшает ли вакцинация показатели выживаемости по сравнению со стандартными методами лечения, отмечают авторы. Усилить клинический эффект и помочь предотвратить развитие резистентности может сочетание вакцины с другими препаратами.
В настоящее время проходят исследования персонализированные мРНК-вакцины компании BioNTech при ранних стадиях других видов рака высокого риска.
Терапевтические вакцины против ВПЧ-ассоциированного рака: структура имеет значение
Телеграм: t.me/ainewsline
Источник: pcr.news