Для запоминания мышам необходимы воспаление и разрывы ДНК в нейронах
МЕНЮ
Главная страница
Поиск
Регистрация на сайте
Помощь проекту
Архив новостей
ТЕМЫ
Новости ИИ
Городские сумасшедшие
ИИ в медицине
ИИ проекты
Искусственные нейросети
Искусственный интеллект
Слежка за людьми
Угроза ИИ
Компьютерные науки
Машинное обуч. (Ошибки)
Машинное обучение
Машинный перевод
Нейронные сети начинающим
Психология ИИ
Реализация ИИ
Реализация нейросетей
Создание беспилотных авто
Трезво про ИИ
Философия ИИ
Генетические алгоритмы
Капсульные нейросети
Основы нейронных сетей
Распознавание лиц
Распознавание образов
Распознавание речи
Творчество ИИ
Техническое зрение
Чат-боты
Авторизация
2024-03-31 13:48

Гиппокамп отвечает за хранение кратковременной памяти и за консолидацию информации. Международная группа ученых нашла новую популяцию нейронов в гиппокампе мышей, отвечающих за формировании контекстуальных воспоминаний. В таких нейронах после того или иного события возникают двухцепочечные разрывы ДНК, присутствие которых активирует рецептор врожденного иммунитета TLR9. У мышей, нокаутных по этому рецептору, нарушалось формирование контекстуальной памяти.
За хранение воспоминаний в мозге отвечают гиппокамп и кора головного мозга. Функция гиппокампа состоит в сохранении кратковременной памяти и в консолидации информации — переводе ее из кратковременной памяти в долговременную. В формировании и хранении воспоминаний задействованы разные популяции нейронов. Например, в гиппокампе, а также в кортексе и в амигдале есть энграммные нейроны, которые участвуют в формировании долговременной памяти. Для этих нейронов характерно кратковременное повреждение ДНК и экспрессия немедленно-ранних генов (immediate early genes, гены раннего ответа), таких как cFos и Egr1, которая регулируется транскрипционным фактором CREB. Теперь международная группа ученых выявила у мышей еще одну популяцию нейронов гиппокампа, которая ответственна за формирование воспоминаний.
Ученые рассматривали, какие изменения происходят в нейронах гиппокампа мышей после выработки условного рефлекса в связи со страхом (fear conditioning). Мышей помещали в специальную установку, где им позволяли освоиться, а потом давали короткий удар током. В норме через 24-48 часов после такого теста в нейронах можно зафиксировать экспрессию немедленно-ранних генов, которая говорит о формировании воспоминания, а при повторных тестах мыши, оказываясь в той же установке, замирают в страхе, помня об ударе током. Исследователи решили узнать, что происходит в нейронах через более длительный срок после такого теста.
Сначала ученые секвенировали РНК клеток гиппокампа мышей через 96 часов или 21 день после теста. Через 21 день в нейронах в основном экспрессировались гены, связанные с ресничками и внеклеточным матриксом, что было связано с формированием перинейрональной сети — структуры, которая окружает синапсы и регулирует синаптическую пластичность. А через 96 часов в основном менялась экспрессия генов, связанных с врожденным иммунным ответом на присутствие нуклеиновых кислот, а также с вырабтокой цитокинов. Среди этих генов наиболее выраженной была экспрессия рецептора TLR9, а также генов, которые участвуют в NF-?B сигналинге, запускающемся после активации этого рецептора.
TLR9 — толл-подобный рецептор, который преимущественно распознает CpG-островки в бактериальной или вирусной ДНК и активируется в ответ на инфекцию. Обычно он локализуется в эндосомах, что наблюдалось и в нейронах гиппокампа. Инфекции у мышей не было, и ученые заподозрили, что TLR9 в нейронах активировался в ответ на фрагменты митохондриальной ДНК, которые могут образовываться при стрессе. Однако изолированные из нейронов фрагменты дцДНК происходили из геномной ДНК, преимущественно из некодирующих регионов.
Эксперименты продолжили с нейронами региона гиппокампа CA1, которые участвуют в формировании и хранении контекстуальных воспоминаний (связанных с определенным контекстом). Действительно, после теста по обуславливанию страха в нейронах происходили двухцепочечные разрывы ДНК и запускалась их репарация. Участки ДНК, в которых выявлялся фосфогистон ?H2AX (маркер двухцепочечных разрывов), сохранялись в течение 6-96 часов после теста, причем только в нейронах, но не в астроцитах или микроглии. Этот процесс сопровождался повреждением ядерной ламины, из-за чего фрагменты ДНК и фосфогистон выбрасывались в перинуклеарное пространство, причем в те его участки, где находился неактивный TLR9. В ответ на повреждение ДНК в таких нейронах также активировался белок 53BP1, участвующий в негомологичном соединении концов (NHEJ). При этом 53BP1, как и часть фосфогистонов и фрагментов ДНК, находились вблизи центромер — вероятно, они задействованы не только в поддержании геномной целостности делящих клеток, но и в формировании памяти.
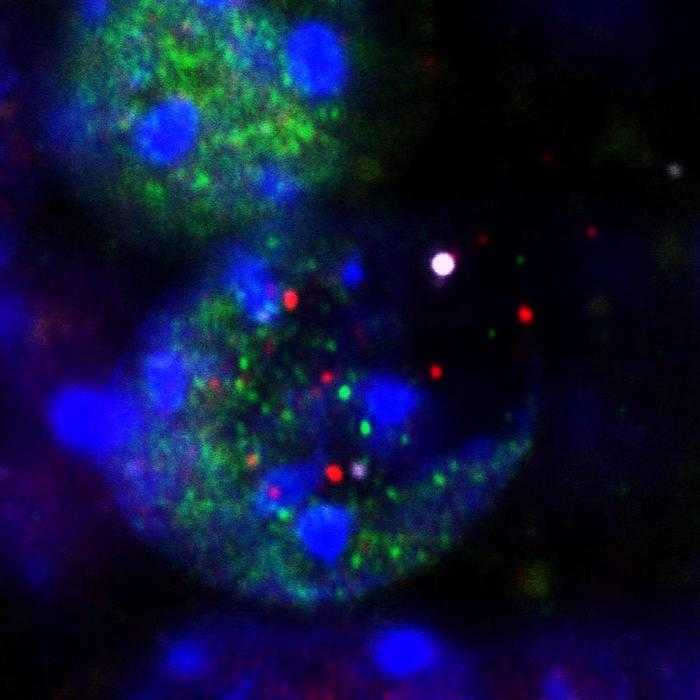
Оказалось, что те нейроны, в которых наблюдается длительное повреждение ДНК, не являются энграммными. В нейронах, где детектировался ?H2AX, практически не были активны Fos, CREB и EGR1. При этом в них активировались сигнальные пути, связанные с воспалением, например, появлялся белок RELA — одна из субъединиц NF-?B. Эти особенности говорили о том, что исследователи имеют дело с новой популяцией нейронов.
Ученые захотели выяснить, вызывается ли воспаление в этих нейронах повреждением ДНК, которое происходит в ответ на обучение, или оно, напротив, необходимо для формирования воспоминаний. Для этого они получили мышей с нейронспецифическим нокаутом по Tlr9 (с помощью рекомбиназы Cre или короткой шпилечной РНК). У таких мышей нарушилась контекстуальная память: когда их помещали в установку, где ранее их били током, они не показывали страха. Аналогичным образом они не привыкали бояться звука, за которым через некоторое время следовал удар тока. Однако в другом тесте, когда мышей били током сразу после звукового сигнала — результаты нокаутных животных не отличались от контрольных, поскольку в этом тесте проверяется обучение, независимое от гиппокампа.
Чтобы подтвердить, что для формирования контекстуальной памяти требуется именно TLR9, а не другой сенсор внеядерной ДНК — cGAS, исследователи применили несколько препаратов, которые действуют тот или другой белок. Так, формирование контекстуальной памяти нарушал олигонуклеотид ODN2088, антагонист TLR9, но не малые молекулы RU-521 и H-151, ингибиторы пути cGAS–STING. На контекстуальную память также не влиял нокаут гена Sting1. Формирование контекстуальных воспоминаний нарушало подавление экспрессии ДНКазы II, которая расщепляет дцДНК на более короткие фрагменты, способные связываться с TLR9 и активировать его. А оверэкспрессия ДНКазы TREX1, которая ограничивает активацию пути cGAS–STING, опять же, не влияла на формирование контекстуальной памяти. Все это означало, что в этом процессе главную роль играет именно TLR9.
Секвенирование РНК отдельных ядер (snRNA-seq) показало, что нокдаун Tlr9 влияет на экспрессию генов после тестов по обуславливанию страха. У контрольных мышей дикого типа через 96 часов после таких тестов повышалась экспрессия генов, ассоциированных с формированием везикул, их транспортом и функцией, а также генов, которые связаны с выработкой интерлейкина-6, с фолдингом TLR9 и его активацией. У мышей с нокдауном Tlr9 их экспрессия не менялась.
Исследователи также показали, что активация TLR9 необходима для нормальной репарации ДНК после тестов на обуславливание страха, для цилиогенеза и для накопления перинейрональной сети. В этой серии экспериментов тесты проходили мыши с нокаутом по Rela и по Ifnar1 (кодирует рецептор интерферона). Через 24 часа после теста у всех мышей, включая контрольную группу, повысилось число нейронов с двухцепочечными разрывами ДНК. Однако у всех нокаутных мышей их было гораздо больше, в том числе у «наивных» мышей, которые не проходили тест по обуславливанию страха. У мышей с нокаутом по Tlr9 и по Rela белок 53BP1 не связывался ни с местами разрывов ДНК, ни с центромерами, что нарушало репарацию ДНК. У тех же мышей хуже формировались реснички и перинейрональная сеть.
Таким образом, исследователи нашли у мышей новую популяцию нейронов гиппокампа, для которой характерен воспалительный ответ, запускаемый через TLR9 в ответ на повреждение ДНК и которая участвует в формировании контекстуальных воспоминаний. TLR9 важен не только для иммунитета, но и для поддержания целостности генома, при его отсутствии нарушается работа системы репарации ДНК. Исследователи предположили, что TLR9, RELA и другие компоненты связанного с ними сигнального пути в будущем могут стать мишенями профилактических и терапевтических препаратов, предназначенных для сохранения когнитивных функций, в том числе при старении и нейродегенерации.
Мыши с расстройством аутистического спектра помнят раннее детство
Источник: pcr.news