Системная красная волчанка: болезнь с тысячью лиц
МЕНЮ
Главная страница
Поиск
Регистрация на сайте
Помощь проекту
Архив новостей
ТЕМЫ
Новости ИИ
Городские сумасшедшие
ИИ в медицине
ИИ проекты
Искусственные нейросети
Искусственный интеллект
Слежка за людьми
Угроза ИИ
ИИ теория
Компьютерные науки
Машинное обуч. (Ошибки)
Машинное обучение
Машинный перевод
Нейронные сети начинающим
Психология ИИ
Реализация ИИ
Реализация нейросетей
Создание беспилотных авто
Трезво про ИИ
Философия ИИ
Генетические алгоритмы
Капсульные нейросети
Основы нейронных сетей
Промпты. Генеративные запросы
Распознавание лиц
Распознавание образов
Распознавание речи
Творчество ИИ
Техническое зрение
Чат-боты
Авторизация
2020-11-28 06:03
Что общего, кроме вклада в музыкальную культуру, казалось бы, может быть у обладательницы семи премий «Грэмми» Тони Брэкстон, современной певицы Селены Гомес и реальной девушки Люси, о существовании которой мир узнал из битловского хита Lucy In The Sky With Diamonds? У всех троих была диагностирована системная красная волчанка (СКВ) — одно из сложнейших аутоиммунных заболеваний, при котором в организме появляются антитела к собственной ДНК. Из-за этого болезнь затрагивает практически весь организм: могут повреждаться любые клетки и ткани, и возникает системное воспаление [1], [2]. Чаще всего страдают соединительные ткани, почки и сердечно-сосудистая система.
Век назад человек с СКВ был обречен [3]. Сейчас, благодаря множеству препаратов, выживаемость пациентов улучшилась: можно облегчить симптомы болезни, уменьшить повреждение органов, повысить качество жизни. В начале и середине 20-го века от СКВ люди умирали скоропостижно, поскольку лечения практически не получали. В 1950-х ожидаемая пятилетняя выживаемость составляла примерно 50% — иными словами, половина пациентов умирала в течение пяти лет. Сейчас же, с появлением современных терапевтических поддерживающих стратегий, выживаемость в течение 5, 10 и 15 лет составляет 96, 93 и 76%, соответственно [4]. Смертность от СКВ значительно варьирует в зависимости от гендерной принадлежности (женщины болеют в разы чаще мужчин, см. рис. 1) [5], этнической группы и страны проживания. Тяжелее всего заболевание протекает у чернокожих мужчин.
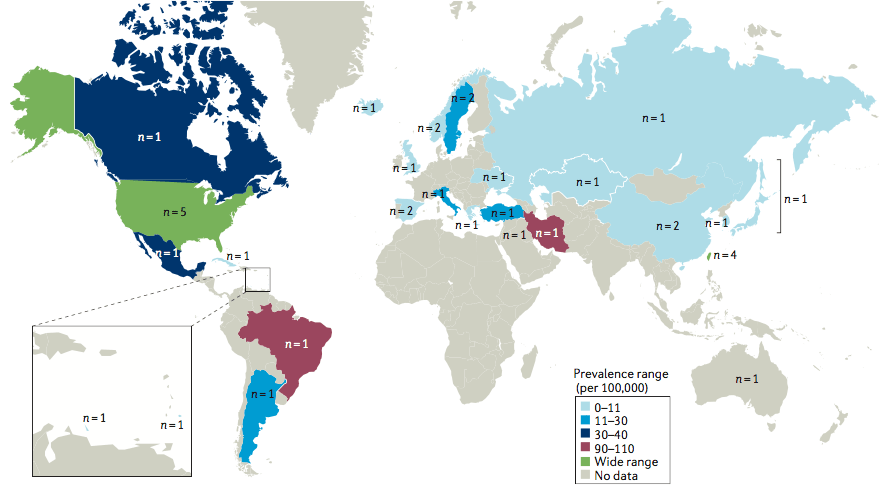
Рисунок 1. Распространенность СКВ. Среди мужчин. Цвет в легенде рисунка отражает количество случаев на 100 000 населения
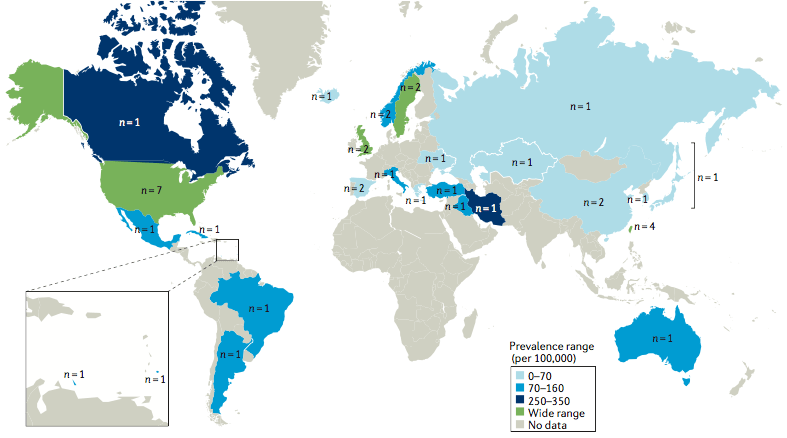
Рисунок 1. Распространенность СКВ. Среди женщин. Цвет в легенде рисунка отражает количество случаев на 100 000 населения
Как проявляется СКВ?
Самое узнаваемое, хотя и не самое частое, проявление СКВ — это сыпь на щеках и переносице. Часто ее называют «бабочкой» из-за формы высыпаний (рис. 2). Однако симптомы заболевания у пациентов формируют разные комбинации и даже у одного человека на фоне лечения могут проявляться волнообразно — то затихая, то вновь вспыхивая. Многие из проявлений болезни крайне неспецифичны — именно поэтому диагностировать волчанку не так-то просто.

Рисунок 2. Сыпь в форме бабочки на переносице и щеках — один из самых узнаваемых, но отнюдь не самых частых симптомов СКВ [7].
Чаще всего к врачу приходит человек, измученный фебрильной лихорадкой (температурой выше 38,5 °C), и именно этот симптом служит ему поводом для обращения к доктору. Суставы у него опухают и болят, всё тело «ломит», лимфатические узлы увеличиваются и доставляют дискомфорт. Пациент жалуется на быструю утомляемость и нарастающую слабость. Среди других симптомов, озвученных на приеме, встречаются язвы во рту, алопеция и нарушение работы желудочно-кишечного тракта [8]. Часто пациент страдает от мучительной головной боли, депрессии, сильной усталости. Его состояние негативно сказывается на работоспособности и социальной жизни. У некоторых пациентов могут проявиться даже аффективные расстройства, когнитивные нарушения, психозы, двигательные расстройства и миастения [9].
Не удивительно, что Йозеф Смолен (Josef Smolen) из Венской городской клинической больницы общего профиля (Wiener Allgemeine Krankenhaus, AKH) на конгрессе 2015 года, посвященном этому заболеванию, назвал системную красную волчанку «самым сложным заболеванием в мире».
Для того чтобы оценить активность болезни и успешность лечения, в клинической практике используется около 10 различных индексов. С их помощью можно отслеживать изменения в выраженности симптомов в течение какого-то отрезка времени. Каждому нарушению присваивается определенный балл, и финальная сумма баллов свидетельствует о тяжести болезни. Первые подобные методики появились в 1980-х, и сейчас их надежность уже давно подтверждена исследованиями и практикой. Самые востребованные из них — это SLEDAI (Systemic Lupus Erythematosus Disease Activity Index), его модификация SELENA SLEDAI, использованная в исследовании Safety of Estrogens in Lupus National Assessment (SELENA), BILAG (British Isles Lupus Assessment Group Scale), индекс повреждения SLICC/ACR (Systemic Lupus International Collaborating Clinics/American College of Rheumatology Damage Index) и ECLAM (European Consensus Lupus Activity Measurement) [10]. В России также пользуются оценкой активности СКВ по классификации В.А. Насоновой [11].
Главные мишени болезни
От атак аутореактивных антител некоторые ткани страдают больше, чем другие. При СКВ особенно часто поражаются почки и сердечно-сосудистая система.
Волчаночный нефрит — воспаление почек — встречается с частотой до 55%. Протекает он по-разному: у некоторых это бессимптомная микроскопическая гематурия и протеинурия, у других — быстро прогрессирующая почечная недостаточность. К счастью, в последнее время долгосрочный прогноз при развитии волчаночного нефрита улучшился благодаря появлению более эффективных поддерживающих препаратов и усовершенствованной диагностики. Теперь большинство пациентов с волчаночным нефритом достигает полной или частичной ремиссии [12].
Аутоиммунные процессы также нарушают работу сосудов и сердца. По самым скромным оценкам, каждая десятая смерть от СКВ вызвана нарушениями кровообращения, развившимися вследствие системного воспаления. Риск ишемического инсульта у пациентов с этой болезнью повышается в два раза, вероятность внутримозгового кровоизлияния — в три раза, а субарахноидального — почти в четыре. Выживаемость после инсульта также гораздо хуже, чем в общей популяции [13].
Совокупность проявлений системной красной волчанки необъятна. У одних пациентов болезнь может затрагивать только кожные покровы и суставы. В других же случаях пациентов выматывают непомерная усталость, нарастающая слабость во всем теле, продолжительная фебрильная температура и когнитивные нарушения. К этому могут добавляться тромбоз и тяжелейшие повреждения органов, такие как терминальная стадия почечной болезни. Из-за таких разных проявлений СКВ называют болезнью с тысячей лиц.
Экономический и социальный аспекты болезни
Человек, заболевший СКВ, страдает не только от биологических и медицинских проявлений болезни. Немалая часть бремени болезни приходится на социальную составляющую, причем она может создавать порочный круг усиления симптоматики.
Так, вне зависимости от пола и этнической принадлежности, бедность, низкий уровень образования, отсутствие медицинской страховки, недостаточные социальная поддержка и лечение способствуют усугублению состояния пациента. Это, в свою очередь, ведет к инвалидности, утрате работоспособности и дальнейшему снижению социального статуса. Всё это значительно ухудшает прогноз болезни.
Не стоит сбрасывать со счетов и то, что лечение СКВ крайне дорого, причем затраты напрямую зависят от тяжести болезни. К прямым расходам относят, например, затраты на стационарное лечение (время, проведенное в больницах и реабилитационных центрах, и связанные с этим процедуры), амбулаторное лечение (лечение прописанными обязательными и дополнительными лекарствами, посещение врачей, лабораторные анализы и прочие исследования, вызовы скорой помощи), хирургические операции, транспортировку в медицинские учреждения и дополнительные медицинские услуги. По оценкам 2015 года, в США больной тратит по всем вышеперечисленным статьям в среднем $ 33 тыс. в год. Если же у него развился волчаночный нефрит, то сумма вырастает больше чем в два раза — до $ 71 тыс.
Косвенные расходы могут быть даже выше прямых, поскольку в них включена потеря работоспособности и инвалидность вследствие болезни. Исследователи оценивают сумму таких потерь в $ 20 тыс. [5].
Патогенез: нарушения в иммунной системе
Долгое время патогенез системной красной волчанки оставался загадкой, однако за последнее десятилетие удалось прояснить несколько основополагающих механизмов. Как и следовало предполагать, здесь оказались замешаны иммунные клетки и молекулы иммунного ответа (рис. 3) [6]. Чтобы лучше понять написанное дальше, рекомендуем обратиться к первой статье этого цикла, описывающей базовые механизмы (ауто)иммунитета: «Иммунитет: борьба с чужими и... своими» [16].
По меньшей мере у 95% пациентов обнаруживаются аутоантитела, распознающие фрагменты собственных клеток организма как чужие (!) и поэтому представляющие опасность. Не удивительно, что центральной фигурой в патогенезе СКВ считают В-клетки, производящие аутоантитела. Эти клетки — важнейшая часть адаптивного иммунитета, обладающая способностью презентировать антигены Т-клеткам и секретирующая сигнальные молекулы — цитокины. Как предполагается, развитие болезни запускается гиперактивностью В-клеток и потерей ими толерантности к собственным клеткам организма. В итоге они генерируют множество аутоантител, которые направлены на ядерные, цитоплазматические и мембранные антигены, содержащиеся в плазме крови. В результате связывания аутоантител и ядерного материала образуются иммунные комплексы, которые откладываются в тканях и эффективно не удаляются. Многие клинические проявления волчанки — результат именно этого процесса и последующего повреждения органов. Воспалительная реакция усугубляется тем, что В-клетки секретируют провоспалительные цитокины и представляют Т-лимфоцитам не чужеродные антигены, а антигены собственного организма [1].
Патогенез заболевания связан и с двумя другими одновременными событиями: с повышенным уровнем апоптоза (программируемой клеточной смерти) лимфоцитов и с ухудшением переработки мусорного материала, возникающего в ходе аутофагии. Такое «замусоривание» организма ведет к разжиганию иммунного ответа по отношению к собственным клеткам.
- Аутофагия
- — процесс утилизации внутриклеточных компонентов и восполнения запаса питательных веществ в клетке — сейчас у всех на устах. В 2016 году за открытие сложной генетической регуляции [17] аутофагии Ёсинори Осуми (Yoshinori Ohsumi) удостоился Нобелевской премии. Роль «самоедства» заключается в поддержании клеточного гомеостаза, переработке поврежденных и старых молекул и органелл, а также в поддержании выживаемости клеток в стрессовых условиях. Подробнее об этом можно почитать в статье на «биомолекуле» [18].
Недавние исследования показывают, что аутофагия важна для нормального протекания множества иммунных реакций: например, для созревания и работы клеток иммунной системы, распознавания патогена, процессинга и презентирования антигена. Сейчас появляется всё больше и больше данных о том, что аутофагические процессы связаны с возникновением, протеканием и тяжестью СКВ.
Было показано, что in vitro макрофаги пациентов с СКВ поглощают меньше клеточных остатков по сравнению с макрофагами здоровых людей из контрольной группы [19]. Таким образом, при неуспешной утилизации апоптотические отходы «привлекают внимание» иммунной системы, и происходит патологическая активация иммунных клеток (рис. 3). Оказалось, что некоторые виды лекарств, которые уже используются для терапии СКВ или находятся на стадии доклинических исследований, действуют именно на аутофагию [20].
Кроме перечисленных выше особенностей, для пациентов с СКВ характерна повышенная экспрессия генов интерферонов типа I. Продукты этих генов — очень известная группа цитокинов, играющих противовирусную и иммуномодулирующую роли в организме. Возможно, увеличение количества интерферонов I типа влияет на активность иммунных клеток, что и ведет к сбою в работе иммунной системы.
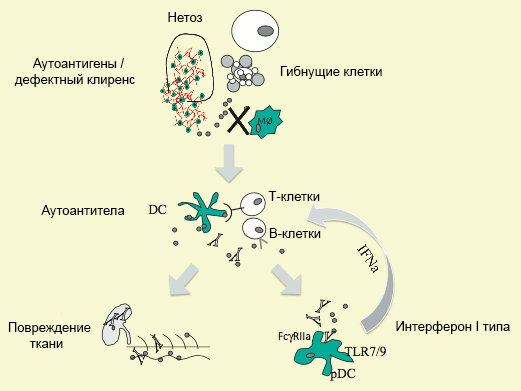
Рисунок 3. Современные представления о патогенезе СКВ. Одна из основных причин клинических симптомов СКВ — отложение в тканях иммунных комплексов, образованных антителами, связавшими фрагменты ядерного материала клеток (ДНК, РНК, гистонов). Этот процесс провоцирует сильную воспалительную реакцию. Кроме того, при усилении апоптоза, нетоза, снижении эффективности аутофагии неутилизированные фрагменты клеток становятся мишенями клеток иммунной системы. Иммунные комплексы посредством рецепторов Fc?RIIa поступают внутрь плазмоцитоидных дендритных клеток (pDC), где нуклеиновые кислоты комплексов активируют Toll-подобные рецепторы (TLR-7/9) [21], [22]. Активированные таким образом pDC приступают к мощной наработке интерферонов I типа (в т.ч. IFN-?). Эти цитокины, в свою очередь, стимулируют созревание моноцитов (M?) до антигенпредставляющих дендритных клеток (DC) и выработку аутореактивных антител В-клетками, предотвращают апоптоз активированных Т-клеток. Моноциты, нейтрофилы и дендритные клетки под действием IFN типа I усиливают синтез цитокинов BAFF (стимулятор В-клеток, способствующий их созреванию, выживанию и продукции антител) и APRIL (индуктор клеточной пролиферации). Всё это ведет к увеличению количества иммунных комплексов и еще более мощной активации pDC — круг замыкается. В патогенез СКВ вовлечен и аномальный метаболизм кислорода, усиливающий воспаление, гибель клеток и приток аутоантигенов. Во многом это вина митохондрий: нарушение их работы ведет к усиленному образованию активных форм кислорода (ROS) и азота (RNI), ухудшению защитных функций нейтрофилов и нетозу (NETosis)
Наконец, свою лепту в развитие болезни может вносить и окислительный стресс вместе с аномальным метаболизмом кислорода в клетке и нарушениями в работе митохондрий. Из-за усиленной секреции провоспалительных цитокинов, повреждения тканей и других процессов, характеризующих течение СКВ, образуется излишнее количество активных форм кислорода (АФК) [23], которые еще сильнее повреждают окружающие ткани, способствуют постоянному притоку аутоантигенов и специфическому самоубийству нейтрофилов — нетозу (NETosis). Этот процесс завершается образованием нейтрофильных внеклеточных ловушек (NETs), предназначенных для улавливания патогенов. К сожалению, в случае СКВ они играют против хозяина: эти сетевидные структуры состоят преимущественно из основных волчаночных аутоантигенов [24]. Взаимодействие с последними антител затрудняет очистку организма от этих ловушек и усиливает производство аутоантител. Так образуется порочный круг: нарастающее повреждение тканей при прогрессировании болезни влечет за собой увеличение количества АФК, что разрушает ткани еще больше [25], усиливает формирование иммунных комплексов, стимулирует синтез интерферона... Детальнее патогенетические механизмы СКВ представлены на рисунках 3 и 4.
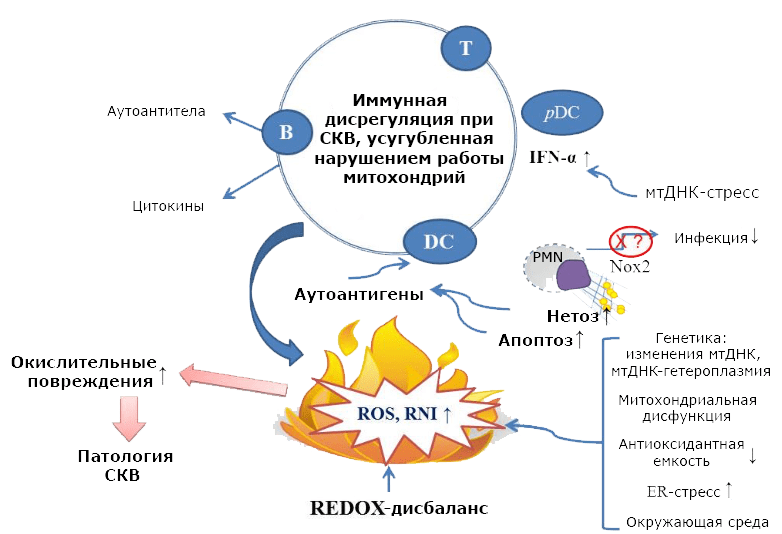
Рисунок 4. Роль программируемой смерти нейтрофилов — нетоза — в патогенезе СКВ. Иммунные клетки обычно не сталкиваются с большинством собственных антигенов организма, поскольку потенциальные аутоантигены находятся внутри клеток и не презентируются лимфоцитам. После аутофагической смерти остатки погибших клеток быстро утилизируются. Однако в некоторых случаях, например, при избытке активных форм кислорода и азота (ROS и RNI), иммунная система сталкивается с аутоантигенами «нос к носу», что провоцирует развитие СКВ. К примеру, под воздействием АФК полиморфноядерные нейтрофилы (PMN) подвергаются нетозу, и из остатков клетки образуется «сеть» (англ. net), содержащая нуклеиновые кислоты и белки. Эта сеть и становится источником аутоантигенов. В результате активируются плазмоцитоидные дендритные клетки (pDC), высвобождая IFN-? и провоцируя аутоиммунную атаку. Прочие условные обозначения: REDOX (reduction—oxidation reaction) — нарушение баланса окислительно-восстановительных реакций; ЭР — эндоплазматический ретикулум; DC — дендритные клетки; B — B-клетки; Т — Т-клетки; Nox2 — NADPH-оксидаза 2; mtDNA — митохондриальная ДНК; черные стрелки вверх и вниз — усиление и подавление соответственно. Чтобы увидеть рисунок в полном размере, нажмите на него.
Кто виноват?
Хотя патогенез системной красной волчанки более-менее ясен, ученые затрудняются назвать ключевую ее причину и потому рассматривают совокупность различных факторов, которые повышают риск развития этой болезни.
В наш век ученые обращают свой взор в первую очередь на наследственную предрасположенность к болезни. Не избежала этого и СКВ — что не удивительно, ведь заболеваемость сильно варьирует по половому и этническому признакам. Женщины страдают от этой болезни примерно в 6–10 раз чаще, чем мужчины. Пик заболеваемости у них приходится на 15–40 лет, то есть на детородный возраст [8]. С этнической принадлежностью связаны распространенность, течение заболевания и смертность. Например, сыпь «бабочкой» типична для белых пациентов. У афроамериканцев и афрокарибцев болезнь протекает гораздо тяжелее, чем у европеоидов, рецидивы болезни и воспалительные нарушения работы почек встречаются у них чаще. Дискоидная волчанка тоже чаще бывает у темнокожих [5].
Эти факты указывают на то, что генетическая предрасположенность может играть важную роль в этиологии СКВ.
Чтобы прояснить это, исследователи использовали метод полногеномного поиска ассоциаций, или GWAS [26], [27], [28], который позволяет соотнести тысячи генетических вариантов с фенотипами — в этом случае с проявлениями болезни. Благодаря этой технологии удалось определить более 60 локусов предрасположенности к системной красной волчанке. Их условно можно разделить на несколько групп. Одна из таких групп локусов связана с врожденным иммунным ответом. Это, например, пути сигналинга NF-kB, деградации ДНК, апоптоза, фагоцитоза, утилизации клеточных остатков. В нее входят и варианты, отвечающие за функцию и сигналинг нейтрофилов и моноцитов. В другую группу попадают генетические варианты, вовлеченные в работу адаптивного звена иммунной системы, то есть связанные с функцией и сигнальными сетями B- и Т-клеток. Кроме того, есть локусы, которые не попадают в эти две группы. Интересно, что многие локусы риска являются общими для СКВ и других аутоиммунных заболеваний (рис. 5).
Генетические данные можно было бы использовать для определения риска развития СКВ, ее диагностики или лечения. Это было бы крайне полезно на практике, поскольку из-за специфики болезни ее не всегда удается выявить по первым жалобам пациента и клиническим проявлениям. Подбор лечения тоже занимает некоторое время, ведь пациенты по-разному отвечают на терапию — в зависимости от особенностей своего генома. Пока, однако, генетические тесты в клинической практике не используют. Идеальная модель для оценки предрасположенности к болезни должна была бы принимать во внимание не только определенные варианты генов, но и генетические взаимодействия, уровни цитокинов, серологических маркеров и многие другие данные. Помимо этого, она должна была бы по возможности учитывать и эпигенетические особенности — ведь именно они, согласно исследованиям, вносят огромный вклад в развитие СКВ [29].
В отличие от генома, эпигеном сравнительно легко модифицируется под влиянием внешних факторов. Некоторые считают, что без них, возможно, СКВ и не развивается. Наиболее очевидный из них — это ультрафиолетовое излучение, поскольку после воздействия солнечного света у пациентов на коже зачастую проявляются покраснения и сыпь.
Развитие болезни, по-видимому, может спровоцировать и вирусная инфекция. Не исключено, что в этом случае аутоиммунные реакции возникают из-за молекулярной мимикрии вирусов — феномена сходства вирусных антигенов с собственными молекулами организма. Если эта гипотеза верна, то тогда в фокус исследований попадает вирус Эпштейна-Барр [30]. Однако в большинстве случаев ученые затрудняются назвать «имена» конкретных виновников. Предполагают, что аутоиммунные реакции провоцируются не конкретными вирусами, а посредством общих механизмов борьбы с этим видом патогенов. К примеру, путь активации интерферонов типа I — общий в ответе на вирусную инвазию и в патогенезе СКВ [6].
Исследовались и такие факторы, как курение и употребление алкоголя, однако их влияние неоднозначно. Вероятно, курение может увеличить риск развития заболевания, обострить его и усилить повреждение органов. Алкоголь же, по некоторым данным, уменьшает риск развития СКВ, однако свидетельства достаточно противоречивы, и этот способ защиты от болезни лучше не использовать [5].
Не всегда есть четкий ответ и относительно влияния профессиональных факторов риска. Если контакт с диоксидом кремния, согласно ряду работ, провоцирует развитие СКВ, то насчет воздействия металлов, промышленных химикатов, растворителей, пестицидов и красок для волос точного ответа пока нет. Наконец, как уже упоминалось выше, волчанку может спровоцировать употребление лекарств: чаще всего триггерами являются хлорпромазин, гидралазин, изониазид и прокаинамид.
Лечение: прошлое, настоящее и будущее
Как уже упоминалось, вылечить «самое сложное заболевание в мире» еще нельзя. Созданию лекарства препятствует многогранный патогенез заболевания, вовлекающий разные части иммунной системы. Однако грамотным индивидуальным подбором поддерживающей терапии можно достичь глубокой ремиссии [31], и пациент сможет жить с красной волчанкой просто как с хронической болезнью.
Лечение при различных изменениях состояния больного может корректироваться врачом, точнее, врачами. Дело в том, что в терапии волчанки крайне важна скоординированная работа мультидисциплинарной группы медицинских профессионалов [32]: семейного врача на Западе, ревматолога, клинического иммунолога, психолога, а зачастую и нефролога, гематолога, дерматолога, невролога. В России больной СКВ в первую очередь поступает к ревматологу, а в зависимости от повреждения систем и органов ему может потребоваться дополнительная консультация кардиолога, нефролога, дерматолога, невролога и психиатра.
Патогенез заболевания очень сложен и запутан, поэтому многие таргетные препараты сейчас находятся в разработке, другие же показали свою несостоятельность на стадии испытаний. Поэтому в клинической практике пока наиболее широко используют неспецифические лекарства.
Стандартное лечение включает несколько типов лекарств. Первым делом выписывают иммунодепрессанты — для того чтобы подавить чрезмерную активность иммунной системы. Самые часто используемые из них — цитостатические препараты метотрексат, азатиоприн, микофенолат мофетила и циклофосфамид. По сути, это те же самые препараты, которые используются для химиотерапии рака и действуют в первую очередь на активно делящиеся клетки (в случае иммунной системы — на клоны активированных лимфоцитов). Понятно, что такая терапия имеет множество опасных побочных эффектов.
В острую фазу болезни пациенты стандартно принимают кортикостероиды — неспецифические противовоспалительные препараты, помогающие унять самые яростные шквалы аутоиммунных реакций. Их используют в терапии СКВ с 1950-х. Тогда они перевели лечение этого аутоиммунного заболевания на качественно новый уровень, и до сих пор остаются основой терапии за неимением альтернативы, хотя с их использованием тоже связано множество побочных эффектов. Чаще всего врачи прописывают преднизолон и метилпреднизолон.
При обострении СКВ с 1976 года также используется и пульс-терапия: больной получает импульсно в высоких дозах метилпреднизолон и циклофосфамид [33]. Конечно, за 40 лет применения схема такой терапии сильно видоизменилась, но до сих пор считается золотым стандартом в лечении волчанки. При этом она дает множество тяжелых побочных эффектов, из-за чего ее не рекомендуют некоторым группам пациентов, например, людям с плохо контролируемой артериальной гипертонией и страдающим системными инфекциями. В частности, у пациента могут развиться метаболические нарушения и измениться поведение.
При достижении ремиссии обычно назначают антималярийные препараты, которые уже долгое время успешно используют для лечения пациентов с поражением опорно-двигательного аппарата и кожи. Действие гидроксихлорохина, одного из самых известных веществ этой группы, например, объясняют тем, что он ингибирует продукцию IFN-?. Его использование обеспечивает долгосрочное снижение активности болезни, уменьшает повреждение органов и тканей и улучшает исход беременности. Кроме того, лекарство снижает риск тромбоза — а это крайне важно, если учитывать осложнения, возникающие в сердечно-сосудистой системе. Так, применение антималярийных препаратов рекомендовано для всех больных СКВ [6]. Однако есть и капля дегтя в бочке меда. В редких случаях в ответ на эту терапию развивается ретинопатия, а больные с тяжелой почечной или печеночной недостаточностью подвержены риску токсического эффекта, связанного с гидроксихлорохином [34].
Используются в лечении волчанки и более новые, таргетные препараты (рис. 5). Самые передовые разработки нацелены на В-клетки: это антитела ритуксимаб и белимумаб.
Ритуксимаб — это химерное моноклональное антитело, применяемое для терапии В-клеточных лимфом. Оно избирательно уничтожает зрелые В-клетки, взаимодействуя с мембранным белком CD20. В отдельных работах была продемонстрирована его эффективность в терапии волчанки, особенно у пациентов с тяжелой формой болезни, когда присутствуют почечные, гематологические и кожные симптомы. Однако в двух ключевых рандомизированных контролируемых исследованиях препарат не показал хороших результатов, поэтому такая терапия официально не рекомендована для лечения СКВ.
Второй препарат оказался гораздо успешнее. В результате исследований выяснилось, что у пациентов с СКВ сывороточные уровни цитокина BAFF/BLyS, стимулирующего B-клетки, гораздо выше, чем у здоровых людей. Сигнальный каскад, в который входит BAFF, является ключевым для развития аутореактивных В-клеток. BAFF контролирует созревание В-клеток, пролиферацию и выработку иммуноглобулина, а гуманизированное моноклональное антитело белимумаб связывает BAFF и тем самым нейтрализует его действие. Безопасность и хорошая переносимость препарата были показаны в исследовании длительностью семь лет, а самыми частыми его побочными эффектами оказались не несущие опасности для жизни инфекции легкой и средней степеней тяжести. Таким образом, белимумаб стал первым препаратом для лечения СКВ с 1956 года — более чем за 60 лет [1], [34], [35]!
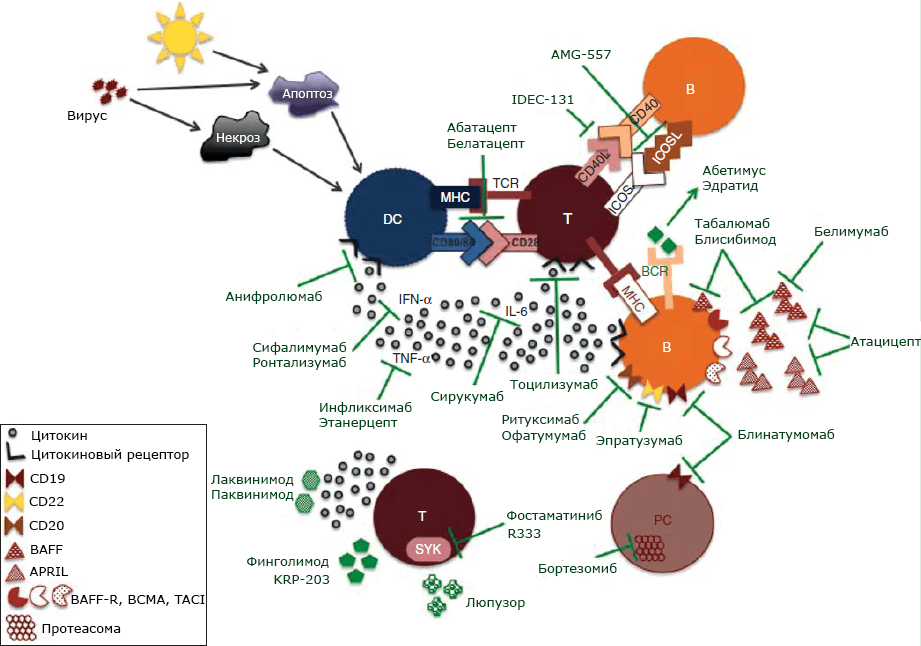
Рисунок 5. Биологические препараты в терапии СКВ. В организме человека накапливаются апоптотические и (или) некротические остатки клеток — например, из-за заражения вирусами и воздействия ультрафиолета. Этот «мусор» может захватываться дендритными клетками (DC), чья основная функция — презентация антигенов Т- и В-клеткам. Последние приобретают способность реагировать и на аутоантигены, представленные им DC. Так и начинается аутоиммунная реакция, запускается синтез аутоантител. Сейчас изучают многие биологические препараты — лекарства, воздействующие на регуляцию иммунных компонентов организма. На врожденную иммунную систему нацелены анифролюмаб (антитело к рецептору IFN-?), сифалимумаб и ронтализумаб (антитела к IFN-?), инфликсимаб и этанерцепт (антитела к фактору некроза опухоли, TNF-?), сирукумаб (анти-IL-6) и тоцилизумаб (анти-IL-6-рецептор). Абатацепт (см. текст), белатацепт, AMG-557 и IDEC-131 блокируют костимуляторные молекулы Т-клеток. Фостаматиниб и R333 — ингибиторы селезеночной тирозинкиназы (SYK). На различные трансмембранные белки B-клеток нацелены ритуксимаб и офатумумаб (антитела к CD20), эпратузумаб (анти-CD22) и блинатумомаб (анти-CD19), который также блокирует рецепторы плазматических клеток (PC). Белимумаб (см. текст) блокирует растворимую форму BAFF, табалюмаб и блисибимод — растворимые и связанные с мембраной молекулы BAFF, а атацицепт — BAFF и APRIL. Некоторые препараты действуют как толерогены, то есть вещества, восстанавливающие толерантность клеток иммунной системы: лаквинимод, паквинимод, финголимод, KRP-203 и люпузор (ригеримод) — для Т-клеток, абетимус и эдратид — для В-клеток. Прочие условные обозначения: BCR — рецептор B-клеток; TCR — рецептор Т-клеток; MHC — главный комплекс гистосовместимости. Чтобы увидеть рисунок в полном размере, нажмите на него.
Еще одна потенциальная мишень антиволчаночной терапии — это интерфероны I типа, о которых уже шла речь выше. Несколько антител к IFN-? уже показали многообещающие результаты у пациентов с СКВ. Сейчас же планируется следующая, третья, фаза их испытаний.
Также из препаратов, эффективность которых при СКВ сейчас изучают, следует упомянуть абатацепт. Он блокирует костимуляторные взаимодействия между Т- и В-клетками, восстанавливая тем самым иммунологическую толерантность.
Наконец, разрабатываются и проверяются различные антицитокиновые препараты, например, этанерцепт и инфликсимаб — специфические антитела к фактору некроза опухоли, TNF-? [34].
Заключение
Системная красная волчанка остается сложнейшим испытанием для пациента, нелегкой задачей для врача и недоисследованной областью для ученого. Однако медицинской стороной вопроса не ст?ит ограничиваться. Это заболевание предоставляет огромное поле для социальных инноваций, поскольку больной нуждается не только в медицинской помощи, но и в различных видах поддержки, включая психологическую. Так, улучшение методов предоставления информации, специализированные мобильные приложения, платформы с доступно изложенными сведениями значительно повышают качество жизни людей с СКВ [36].
Немало в этом деле помогают и пациентские организации — общественные объединения людей, страдающих каким-то заболеванием, и их родственников. К примеру, очень известна Lupus Foundation of America. Деятельность этой организации направлена на улучшение качества жизни людей с диагнозом СКВ посредством специальных программ, научных исследований, просветительства, поддержки и помощи. В ее первостепенные задачи входит сокращение времени на постановку диагноза, обеспечение пациентов безопасным и эффективным лечением и расширение доступа к лечению и уходу. Помимо этого, организация подчеркивает важность обучения медицинского персонала, донесения проблем до представителей власти и повышения социальной сознательности относительно системной красной волчанки.
Подробнее о структуре, работе и роли подобных организаций речь пойдет в заключительной статье этого цикла.
Литература
- Jyoti Bakshi, Mediola Ismajli, Anisur Rahman. (2015). New therapeutic avenues in SLE. Best Practice & Research Clinical Rheumatology. 29, 794-809;
- Загадочная генетика «загадочной болезни кожи» — витилиго;
- Пасеро Г. и Марсон П. (2008). История изучения системной красной волчанки. Научно-практическая ревматология. 4;
- Fors Nieves C.E. and Izmirly P.M. (2016). Mortality in systemic lupus erythematosus: an updated review. Curr. Rheumatol. Rep. 18, 21;
- Erin E. Carter, Susan G. Barr, Ann E. Clarke. (2016). The global burden of SLE: prevalence, health disparities and socioeconomic impact. Nat Rev Rheumatol. 12, 605-620;
- A. A. Bengtsson, L. R?nnblom. (2017). Systemic lupus erythematosus: still a challenge for physicians. J Intern Med. 281, 52-64;
- Norman R. (2016). The history of lupus erythematosus and discoid lupus: from Hippocrates to the present. Lupus Open Access. 1, 102;
- Lam G.K. and Petri M. (2005). Assessment of systemic lupus erythematosus. Clin. Exp. Rheumatol. 23, S120—132;
- M. Govoni, A. Bortoluzzi, M. Padovan, E. Silvagni, M. Borrelli, et. al.. (2016). The diagnosis and clinical management of the neuropsychiatric manifestations of lupus. Journal of Autoimmunity. 74, 41-72;
- Juanita Romero-Diaz, David Isenberg, Rosalind Ramsey-Goldman. (2011). Measures of adult systemic lupus erythematosus: Updated Version of British Isles Lupus Assessment Group (BILAG 2004), European Consensus Lupus Activity Measurements (ECLAM), Systemic Lupus Activity Measure, Revised (SLAM-R), Systemic Lupus Activity Questi. Arthritis Care Res. 63, S37-S46;
- Педиатрия. Национальное руководство. Т. 1 / Под ред. Баранова А.А. ГЭОТАР-Медиа, 2009. — 1024 с.;
- Maria Grazia Lazzaroni, Francesca Dall’Ara, Micaela Fredi, Cecilia Nalli, Rossella Reggia, et. al.. (2016). A comprehensive review of the clinical approach to pregnancy and systemic lupus erythematosus. Journal of Autoimmunity. 74, 106-117;
- Marie Holmqvist, Julia F Simard, Kjell Asplund, Elizabeth V Arkema. (2015). Stroke in systemic lupus erythematosus: a meta-analysis of population-based cohort studies. RMD Open. 1, e000168;
- Kam Lun Hon, Alexander K. C. Leung. (2012). Neonatal Lupus Erythematosus. Autoimmune Diseases. 2012, 1-6;
- Elaine L. Alexander, Thomas T. Provost. (1981). Ro (SSA) and La (SSB) antibodies. Springer Semin Immunopathol. 4, 253-273;
- Иммунитет: борьба с чужими и… своими;
- Takeshige K., Baba M., Tsuboi S., Noda T., Ohsumi Y. (1992). Autophagy in yeast demonstrated with proteinase-deficient mutants and conditions for its induction. J. Cell Biol. 119 (2), 301–311;
- Нобелевская премия по медицине и физиологии 2016: за самоедство;
- S W Tas. (2006). Macrophages from patients with SLE and rheumatoid arthritis have defective adhesion in vitro, while only SLE macrophages have impaired uptake of apoptotic cells. Annals of the Rheumatic Diseases. 65, 216-221;
- Xiao Liu, Haihong Qin, Jinhua Xu. (2016). The role of autophagy in the pathogenesis of systemic lupus erythematosus. International Immunopharmacology. 40, 351-361;
- Иммунологическая Нобелевская премия (2011);
- Толл-подобные рецепторы: от революционной идеи Чарльза Джейнуэя до Нобелевской премии 2011 года;
- Активный кислород: друг или враг, или О пользе и вреде антиоксидантов;
- Википедия: «Нетоз»;
- Hui-Ting Lee, Tsai-Hung Wu, Chen-Sung Lin, Chyou-Shen Lee, Yau-Huei Wei, et. al.. (2016). The pathogenesis of systemic lupus erythematosus - From the viewpoint of oxidative stress and mitochondrial dysfunction. Mitochondrion. 30, 1-7;
- GWAS и психогенетика: консорциумы в поисках ассоциаций;
- Генетика псориаза: иммунитет, барьерная функция кожи и GWAS;
- Загадочная генетика «загадочной болезни кожи» — витилиго;
- Maria Teruel, Marta E. Alarc?n-Riquelme. (2016). The genetic basis of systemic lupus erythematosus: What are the risk factors and what have we learned. Journal of Autoimmunity. 74, 161-175;
- От поцелуя до лимфомы один вирус;
- Соловьев С.К., Асеева Е.А., Попкова Т.В., Клюквина Н.Г., Решетняк Т.М., Лисицына Т.А. и др. (2015). Стратегия лечения системной красной волчанки «До достижения цели» (teat-to-target SLE). Рекомендации международной рабочей группы и комментарии российских экспертов. Научно-практическая ревматология. 53 (1), 9–16;
- Решетняк Т.М. Системная красная волчанка. Сайт ФГБНУ НИИ ревматологии им. В.А. Насоновой;
- Morton Scheinberg. (2016). The history of pulse therapy in lupus nephritis (1976–2016). Lupus Sci Med. 3, e000149;
- Jordan N. and D’Cruz D. (2016). Current and emerging treatment options in the management of lupus. Immunotargets Ther. 5, 9-20;
- Впервые за полвека появилось новое лекарство от волчанки;
- Tani C., Trieste L., Lorenzoni V., Cannizzo S., Turchetti G., Mosca M. (2016). Health information technologies in systemic lupus erythematosus: focus on patient assessment. Clin. Exp. Rheumatol. 34, S54—S56;
- Andreia Vilas-Boas, Jyoti Bakshi, David A Isenberg. (2015). What can we learn from systemic lupus erythematosus pathophysiology to improve current therapy?. Expert Review of Clinical Immunology. 11, 1093-1107.
Телеграм: t.me/ainewsline
Источник: biomolecula.ru