Пренатальное развитие иммунной системы человека
МЕНЮ
Главная страница
Поиск
Регистрация на сайте
Помощь проекту
Архив новостей
ТЕМЫ
Новости ИИ
Городские сумасшедшие
ИИ в медицине
ИИ проекты
Искусственные нейросети
Искусственный интеллект
Слежка за людьми
Угроза ИИ
ИИ теория
Компьютерные науки
Машинное обуч. (Ошибки)
Машинное обучение
Машинный перевод
Нейронные сети начинающим
Психология ИИ
Реализация ИИ
Реализация нейросетей
Создание беспилотных авто
Трезво про ИИ
Философия ИИ
Генетические алгоритмы
Капсульные нейросети
Основы нейронных сетей
Промпты. Генеративные запросы
Распознавание лиц
Распознавание образов
Распознавание речи
Творчество ИИ
Техническое зрение
Чат-боты
Авторизация
2020-06-26 17:20

Аннотация
Кровь и иммунная система в период раннего эмбриогенеза развиваются параллельно. Возникающие при этом очаги гемопоэза, разделенные в анатомическом пространстве и времени, дают начало циркулирующим и резидентным иммунным клеткам. Предыдущие исследования основывались на животных моделях, которые отличаются от людей как сроками развития, так и набором микроорганизмов, с которыми они взаимодействуют. Определение состава иммунной системы человека в настоящее время возможно благодаря использованию мультиомиксного подхода к единичной клетке. Крупномасштабная одноклеточная геномика, технологии визуализации и инициатива Human Cell Atlas вместе позволили осуществить картирование на уровне развивающейся иммунной системы человека и возникающих в ходе развития свойств. Хотя точные роли специфических иммунных клеток в процессе эмбриогенеза требуют дальнейшего изучения, система в целом проявляет гибкие свойства и высокую чувствительность в соответствии с потребностями развития и проблемами окружающей среды.
Животные модельные системы предоставили фундаментальные доказательства, которые формируют наше понимание процесса развития гемопоэза. Исследования, проведенные на мышах, рыбах данио-рерио и курах, показали, что гемопоэз и иммунногенез происходят в разных анатомических участках (рис. 1). Первые клетки крови развиваются вне зародыша и в условиях тесной связи с эндотелиальными клетками желточного мешка [1]. Эмбриональные гемопоэтические стволовые клетки (ЭГСК), способные репопулировать при трансплантации в организм взрослого хозяина, происходят из области аорто-гонадо-мезонефроса (АГМ) [2]. Печень и костный мозг плода (КМ) впоследствии наполняются как предшественниками, полученными из желточного мешка, так и ЭГСК, поступающими из АГМ [3].
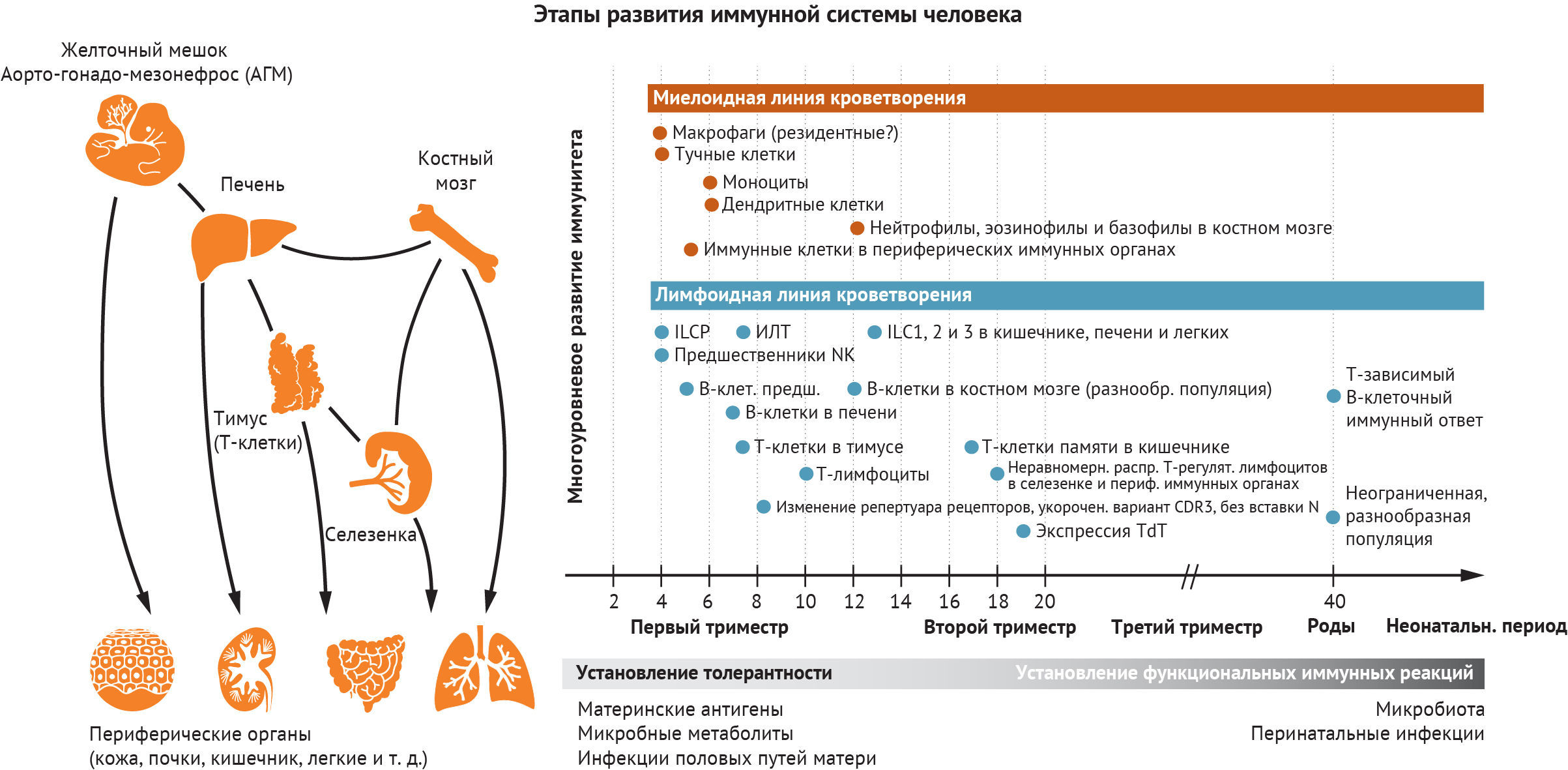
Рисунок 1 | Временное и пространственное развитие иммунной системы человека
Гемопоэз и развитие иммунной системы в начале жизни происходит в нескольких анатомических пространствах. Основной сайт кроветворения изменяется от внеэмбрионального желточного мешка до внутриэмбрионального АГМ, печени и КМ. Дифференцировка и созревание Т-клеток ограничены тимусом. Иммунные клетки заселяют другие лимфоидные и периферические органы, включая лимфатические узлы, кожу, кишечник, почки и легкие, и адаптируются к среде соответствующего органа. Различные типы иммунных клеток развиваются и созревают на разных стадиях беременности, что необходимо для установления иммунологической толерантности и функциональной реакции на основе потребностей развития. Это подготавливает развивающийся эмбрион и плод к воздействию антигенов как во время беременности, так и после родов. ILCP, предшественник ILC; CDR3, дополнительная определяющая область 3; TdT, терминальная дезоксинуклеотидилтрансфераза.
Однако сроки развития иммунной системы неодинаковы у разных видов. Например, тимус плода мыши заметно менее развит по сравнению с таковым у человека, что создает условия для полной дифференцировки наивных Т-клеток в утробе матери [4]. Кроме того, некоторые маркеры, определяющие популяцию тех или иных лимфоцитов, сохраняются недостаточно хорошо, что затрудняет непосредственное применение результатов исследований на животных к людям. Влияние микробной экспозиции системы «мать-плод» на иммунное развитие плода признается научным сообществом все чаще; и как комменсальный, так и патогенный состав микробиоты у разных видов может различаться. Исследования, направленные на изучение развития иммунной системы человека, были затруднены из-за сложного доступа к тканям, а также вследствие экспериментальных и этических ограничений, но мультиомиксные технологии, направленные на анализ единичных клеток, ускорили появление новых открытий. В данном обзоре мы обсуждаем, как эти технологии позволяют получить беспрецедентное представление о внутриутробном развитии иммунной системы. Мы опишем ключевые идеи о том, как меняется иммуногенез во времени и пространстве, и объясним, как иммунные клетки подготавливают плод к взаимодействию с антигеном, а также играют неканонические роли в иммуногенезе.
От отдельных клеток к развитию на уровне системы
Для того, чтобы проанализировать развитие элементов крови ииммунной системы в пренатальном периоде, необходимs высокоэффективные средства. Секвенирование РНК единичных клеток (scRNA-seq) стало мощным инструментом для комплексного понимания иммунной системы, позволяя объективно определять состояние клеток и изучать сложные и гетерогенные многоклеточные структуры [5]. Методы капельного секвенирования scRNA-seq, такие как 10X, теперь масштабируются до такой степени, что становится возможным адекватно проанализировать целые органы. Так, авторы создали профили отдельных клеток из желточного мешка и печени для реконструкции раннего кроветворения, из тимуса — для изучения развития Т-клеток, из кожи и почек — для выяснения заселения иммунными клетками периферических органов [4, 6]. Вычислительные методы позволили сравнить состояния клеток в разных тканях и предсказать важнейшие взаимодействия рецепторов и соответствующих лигандов, которые играют критическую роль в формировании судьбы иммунных клеток в определенных тканях [7].
Корреляция с методами визуализации — например, транскриптомикой in situ, — позволила провести комплексную характеристику микроокружения тканей [4, 7–9]. Траектории развития были прослежены по отдельности для каждой ткани, так как клетки просматривались на разных стадиях дифференцировки и путем интеграции образцов из разных гестационных возрастов. Этот метод позволяет осуществить всестороннее изучение внутриутробного развития иммунитета. Между тем, на сегодняшний день сохраняются значительные проблемы в отслеживании происхождения определенных иммунных клеток по отдельным очагам кроветворения. Достижения в секвенировании ДНК единичных клеток в сочетании с аналитическими методами для отслеживания различных клонов могут приблизить исследователей к этой цели.
Развитие иммунной системы в пространстве и времени
В этом разделе мы рассмотрим ход развития иммунной системы человека в пространстве и времени. Мы начнем с характеристики типов клеток по мере их появления в желточном мешке или печени плода, а затем рассмотрим тимус как ключевой орган, где происходит развитие Т-клеток. Это, к сожалению, не будет исчерпывающим описанием иммуногенеза, поскольку на сегодняшний день в иммунокомпетентных органах и тканях идентифицировано около 40 различных состояний иммунных клеток. Вместо этого мы сосредоточимся на понимании того, как мультиомиксные подходы к изучению одной клетки продвинули понимание функционирования всей иммунной системы плода человека (рис. 2).
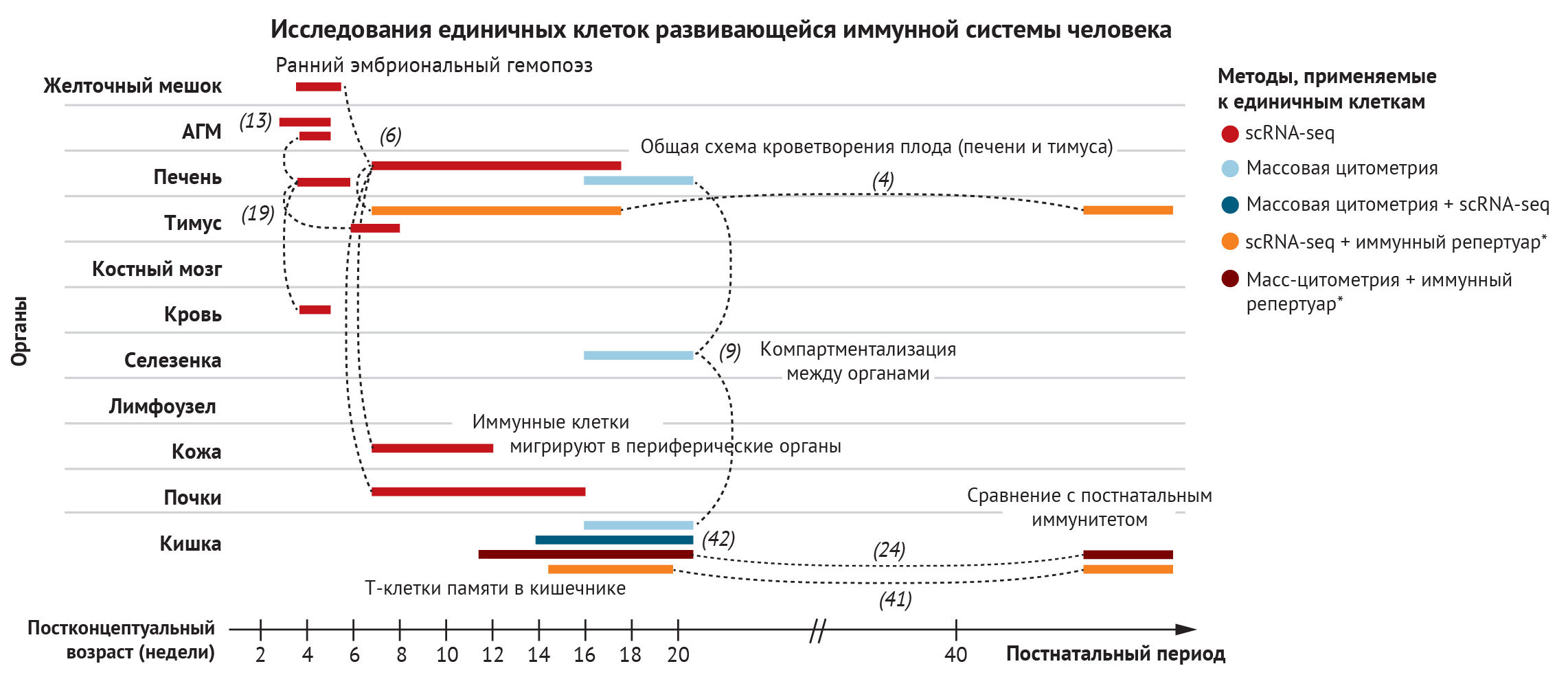
Рисунок 2 | Обзор исследований единичных клеток, детализирующих развитие иммунной системы человека
Для создания всеобъемлющего атласа развития иммунной системы человека были применены разнообразные клеточные методы (изображены в цвете). Во многих исследованиях отбирали сразу несколько органов с целью изучения миграции, адаптации и компартментализации иммунных клеток. (Исследования обозначены референс-номером, а пунктирные линии связывают различные органы, отобранные в каждом исследовании).
Желточный мешок и аорто-гонадо-мезонефрос
Анализ эмбрионального желточного мешка человека демонстрирует присутствие ЭГСК-подобных предшественников, макрофагов, тучных клеток (ТК), предшественников натуральных киллеров (NK) и лимфоидных клеток врожденного иммунитета (ЛВИ) наряду с мегакариоцитами и эритроидными клетками уже на четвертой неделе внутриутробного развития (ВУР) [6]. Происхождение макрофагов интенсивно изучалось, потому что тканевые макрофаги возникают независимо от ЭГСК и способны к самообновлению в условиях гомеостаза на мышиных моделях [10]. Тканерезидентные макрофаги в печени, легких, мозге и эпидермисе, как было показано с помощью картирования развития клеток, возникают в процессе гемопоэза в желточном мешке из эритромиелоидного предшественника [11, 12]. И хотя остаточный вклад желточного мешка сохраняется в ряде тканей (например, в печени, головном мозге и эпидермисе), макрофаги постепенно замещаются моноцитами, происходящими из ЭГСК, и в других местах (например, в кишечнике, легких и сердце).
Этот процесс отчасти зависит от того, насколько «открытой» остается ниша для циркулирующих клеток [10]. У мышей точный вклад первой и второй волн гемопоэза из желточного мешка и ответ на вопрос о возникновении макрофагов из моноцитов до сих остаются неизвестными [10]. При развитии эмбриона у человека тканеспецифичные макрофаги можно наблюдать с самых ранних временных точек [6, 13, 14]. Одноклеточная диссекция АГМ эмбриона человека выявила определенную гемогенную эндотелиальную популяцию, которая дает начало макрофагам [13]. К 6 неделе ВУР эмбриональная поджелудочная железа уже содержит макрофаги, микроглия сопровождает развивающийся мозг, а клетки Хофбауэра выстилают плаценту [7,14,15]. Идентификация этих клеток в значительных количествах до начала гемопоэза в печени плода на 6–9 неделе ВУР свидетельствует о заселении периферических тканей макрофагами, происходящими из желточного мешка или АГМ. Попытки использовать транскрипционное сходство между макрофагами желточного мешка и макрофагами печени плода для анализа онтогенеза макрофагов в тканях недостаточно надежны вследствие влияния окружения на экспрессию генов после оседания этих клеток в тканях.
Однако данный анализ позволил охарактеризовать разнообразие макрофагов, существенно важное для развития, например, макрофагов эритроидных островков, обеспечивающих стимуляцию эритропоэза и клеток Купфера с ярко выраженной фагоцитарной активностью в печени плода [6]. Кроме того, помимо макрофагов, картирование развития клеток показало, что ТК у мышей возникают как из желточного мешка, так и из предшественников, происходящих из ЭГСК, и что паттерны удержания ТК, происходящих из желточного мешка, являются тканеспецифичными [16, 17]. В развитии человека четкий профиль ТК выявляется как в желточном мешке, так и в печени плода [6]. ТК соединительной ткани в коже и почках плода обнаруживают значительное сходство с ТК фетальной печени по профилю экспрессии генов [6]. Эта ранняя «ориентированность» эмбриона н производство ТК вызывает удивление. Наиболее характерной функцией этих клеток является их участие в аллергических реакциях на связывание иммуноглобулина E (IgE) с помощью высокоаффинного рецептора IgE [18]. ТК печени и желточного мешка плохо приспособлены для этой задачи, поскольку они не экспрессирует ген альфа-субъединицы рецептора IgE (FCER-1-A) [6]. Ранняя продукция ТК может происходить для заселения развивающихся участков слизистой оболочки и соединительных тканей резидентными иммунными клетками или же для создания пула эффекторов врожденного иммунитета, способных реагировать на ассоциированные с патогеном молекулярные паттерны. Кроме того, предсказаны и дополнительные функции, заключающиеся в том, что ТК могут способствовать ангиогенезу. У эмбрионов мышей ТК кожи экспрессируют гены, участвующие в формировании паттернов сосудов и нервов [6, 16]. У взрослых млекопитающих ТК поддерживают как физиологический, так и воспалительный ангиогенез [18].
Роль тучных клеток в пренатальном развитии сосудов требует дальнейшего изучения. NK-клетки, предшественники ЛВИ и их общие лимфоидные предшественники могут быть идентифицированы по транскриптому отдельных клеток желточного мешка и печени плода [6, 19]. На более поздних стадиях они обнаруживаются уже с большей степенью разнообразия и дифференцировки в различных фетальных органах [9, 20]. В отличие от материнских децидуальных NK-клеток, роль которых во время беременности хорошо охарактеризована [7, 21], понимание функции фетальных NK-клеток на сегодняшний день ограничено. Хотя NK-клетки плода считаются незрелыми и гипореактивными по сравнению с NK-клетками у взрослых, они уже обладают высокой степенью киллерной активности [22, 23]. Более того, NK-клетки плода или младенца сходны с таковыми у взрослых по целому ряду признаков, что позволяет предположить, что они уже могут реагировать на соответствующие стимулы, такие как, например, вирусная инфекция [23]. Соответственно, NK-клетки в изобилии присутствуют в кишечнике младенцев, содержат цитолитические гранулы, а их способность к дегрануляции превышает таковую у NK-клеток кишечника взрослого человека [20]. В дополнение к NK-клеткам было показано, что и другие типы ЛВИ у плода присутствуют в большем количестве, чем у младенцев [24]. В их числе — клетки-индукторы лимфоидной ткани (ИЛТ), которые играют важнейшую роль в формировании вторичных лимфоидных органов [25, 26]. Взаимодействуя со стромальными клетками, клетки ИЛТ индуцируют положительную обратную связь для привлечения дополнительных клеток ИЛТ и других иммунных клеток, создавая лимфоидное окружение [27]. Таким образом, ЛВИ развиваются у эмбриона человека очень рано и участвуют как в защите тканей, так и в их ремоделировании. В этой наиболее ранней стадии гемопоэза в желточном мешке значительная роль отводится развитию иммунных клеток со структурными и физиологическими функциями наряду с приобретением эмбрионом базового набора врожденных эффекторов иммунитета. Точная роль этих клеток в развитии тканей и участие в прохождении контрольных точек, которые предотвращают повреждающие иммунные реакции в утробе матери, требует дальнейшего изучения.
Печень и костный мозг
Дефинитивные ЭГСК могут генерировать полный набор линий эритроидных, миелоидных, лимфоидных клеток и мегакариоцитов в печени плода, однако нейтрофилы будут отсутствовать до установления гемопоэза в костном мозге (КМ) [28]. В отличие от макрофагов, моноциты и дендритные клетки (ДК) считаются ЭГСК-зависимыми популяциями. У мышей они прослеживаются вплоть до клоногенного предшественника в КМ, называемого предшественником ДК-макрофагов [29]. В процессе человеческого эмбриогенеза первые признаки пролиферации ДК наблюдаются в печени плода уже примерно с 6 недели ВУР [6]. Обычные ДК1, ДК2 и плазмоцитоидные ДК обнаруживаются в тканях плода — включая легкие, селезенку, кожу и тимус — на 12 недели ВУР и являются относительно многочисленными по сравнению с популяцией ДК во взрослых тканях [30]. ДК плода, как и их аналоги во взрослом организме, способны мигрировать, реагировать на Toll-подобные рецепторы и стимулировать пролиферацию и активацию T-клеток [30]. Фетальные ДК обладают особой способностью индуцировать дифференцировку регуляторных Т-лимфоцитов, стимулировать выработку Т-клеточного интерлейкина 4 и ингибировать выработку фактора некроза опухоли альфа (TNF-?) с помощью аргиназы II [30]. Таким образом, ДК играют важную роль в поддержании толерантности во время ВУР. Популяция В-клеток впервые появляется в печени плода с 7 недели ВУР в виде предшественников В-лимфоцитов; зрелые же B-клетки присутствуют только после 9 недели ВУР [6].
Частично это можно объяснить изменением способности ЭГСК продуцировать B-клетки и соответствующего микроокружения печени, необходимого для их дифференцировки [30]. В середине беременности КМ становится основным источником B-клеток, а зрелые B-клетки в изобилии обнаруживаются в селезенке [31]. И хотя разнообразие эмбриональных В-лимфоцитов достигается еще на ранних стадиях [24, 32], формирование герминативных центров подавляется до воздействия антигенов после рождения, что сопровождается активной соматической гипермутацией [33]. Сравнение В-клеток кишечника, полученных от плодов второго триместра, с В-клетками младенцев при помощи масс-цитометрии, комбинированной с анализом репертуара рецепторов В-клеток, хорошо продемонстрировало, что кишечные В-клетки у плода — это, прежде всего, фолликулярные и переходные В-клетки, тогда как плазматические В-клетки в большей степени представлены у младенцев [24]. Другим интересным аспектом дифференцировки В-клеток, который интенсивно изучался на мышиной модели, является поэтапное развитие клеток В-1, сходных с клетками врожденного иммунитета. Они преобладают в начале беременности, а затем появляются и обычные клетки В-2 [34]. Однако окончательно идентичность человеческих B-1-подобных клеток еще не определена [35]. Будущие исследования по созданию клеточного атласа КМ и селезенки плода человека позволят лучше понять онтологию B-клеток, подчеркнув специфические для тех или иных органов различия в нишевых факторах, которые поддерживают дифференцировку B-клеток.
«Клинические последствия иммунного развития и функции плода выходят далеко за пределы жизни в утробе матери»
Тимус и периферические иммунные органы
Тимус обеспечивает среду, необходимую для развития Т-клеток. Ранние лимфоидные предшественники, происходящие из печени плода, мигрируют в тимус на 8 неделе ВУР, где они развиваются в наивные Т-клетки [36]. Развитие и созревание вилочковой железы (тимуса) опосредовано взаимодействием между стромальными клетками тимуса и иммунными компонентами и было в значительной степени изучено на мышиных моделях. Комплексное профилирование транскриптома единичных клеточных компонентов развивающегося тимуса человека показало четкую взаимосвязь между эпителиальными клетками тимуса, клетками мезенхимы, ранними предшественниками тимоцитов, развивающимися и зрелыми Т-клетками и другими популяциями иммунных клеток [4, 19]. Количественные соотношения разных клеточных популяций также демонстрируют скоординированные изменения в процессе развития, что еще раз доказывает важность взаимодействий между несколькими типами клеток для правильного развития органов [4]. Исследования клеток печени и тимуса плода позволили подробно описать молекулярные характеристики, сопровождающие переход от ранних предшественников тимуса к наивным Т-клеткам [4, 6, 19]. Ху и его коллеги сосредоточились на составлении молекулярного профиля клеток-предшественниц, населяющих тимус [19]. Группа авторов данного обзора расширила этот анализ до более поздних этапов развития [4].
Вместе эти исследования выявили непрерывный ряд развития от ранних предшественников тимуса до разнообразных типов зрелых Т-клеток. Наивные Т-клетки выходят из вилочковой железы и мигрируют в другие ткани. Циркулирующие Т-клетки обнаруживаются у плода уже через 10–11 недель после функционального развития тимуса [37]. Отсутствие или наличие микроорганизмов в плодном окружении пока остается предметом дискуссий. Хотя считается, что при нормальном течении беременности это окружение, скорее всего, стерильно, ненаследуемые материнские аллоантигены и побочные продукты обмена микробиоты могут потенциально активировать иммунную систему плода. Чтобы избежать аллореактивности, плод должен поддерживать иммунологическую толерантность. Как следствие, наивные Т-клетки, возникающие у плода, с большей вероятностью приобретают судьбу Т-регуляторных по сравнению со наивными Т-клетками взрослого организма [38]. Фетальные регуляторные Т-клетки подавляют пролиферацию и секрецию цитокинов другими фетальными Т-клетками, которые потенциально обладают самореактивностью [39].
Т-клетки памяти были обнаружены в кишечнике плода, что подчеркивает способность фетальных Т-клеток реагировать на чужеродные антигены [9, 24, 40, 421]. Исследования CD4+ T-лимфоцитов кишечника с помощью технологий анализа единичных клеток в сочетании с определением репертуара клеточных рецепторов выявили существование пула T-клеток памяти и регуляторных T-клеток с признаком клональной экспансии, что демонстрирует баланс между активацией и подавлением адаптивного иммунного ответа у плода [24, 42]. CD4+ Т-клетки кишечника также могут играть роль в стимуляции дифференцировки, как показано в случае умеренной экспрессии TNF-? [41]. Таким образом, адаптивный иммунитет плода оказывается значительно более зрелым, чем предполагалось ранее. Области будущих исследований иммунной системы плода включают изучение антигенных сигналов, лежащих в основе активации фетальных Т-клеток, и роли, которую они играют в развитии и защите плода. При помощи такого анализа онтогенеза иммунитета плода во времени и пространстве авторы отмечают появление как врожденных, так и адаптивных иммунных клеток с характерными свойствами, отличающимися от таковых у взрослых. Среди компонентов, отсутствующих в этом обзоре, можно назвать нейтрофилы. Последние данные свидетельствуют о том, что около трети эмбриональных клеток костного мозга являются нейтрофилами или их предшественниками уже к 10–13 неделе ВУР, и доля их увеличивается до двух третей к 21 неделе ВУР [43]. Младенцы, рожденные недоношенными или маловесными, имеют меньшее количество циркулирующих нейтрофилов, более низкий нейтрофильный пул и более высокой риск смерти от сепсиса [44]. Понимание работы нейтрофильного компартмента у плода , даст представление о том, как можно поддерживать иммунную защиту в раннем возрасте.
Заключение
Мульти-«омиксные» и пространственные технологии предоставили идеальные платформы для подробного анализа и реконструирования развивающейся иммунной системы [4, 6, 9, 13, 19, 24, 41, 42]. Однако многие аспекты остаются неизученными (рис. 3). Как изменяются гемопоэтические предшественники в процессе развития? Как различные тканевые ниши, такие как желточный мешок, печень, КМ, тимус и селезенка, влияют на популяции предшественников и развитие иммунных клеток? Как иммунные клетки мигрируют и адаптируются в периферических нелимфоидных тканях? Как иммунная система взаимодействует с организмом, обучается и формирует память для будущих встреч с антигеном? Завершение разработки иммунного атласа путем сосредоточения внимания на органах и недостающих временных точках, расширение анализа для сравнения со иммунными клетками взрослого организма, а также системное и межвидовое сравнение дадут дополнительные знания о том, как развивалась и развивается иммунная система человека. Клиническое значение понимания развития и функционирования иммунной системы плода выходят далеко за пределы жизни в утробе матери. Характерные для плода гемопоэтические клетки-предшественники в настоящее время признаны вероятными источниками происхождения бластных клеток опухолей системы крови, включая острый мегакариобластический лейкоз, ассоциированный с синдромом Дауна, ювенильный миеломоноцитарный лейкоз и острый лимфобластический лейкоз у детей. Ранние первичные иммунодефицитные состояния с нарушением реакции на заражение патогеном и/или аутоиммунные патологии также могут зависеть от нарушений процесса развития. В этих условиях аберрантный гемопоэз также приводит к изменению функционирования иммунной системы. Биологическое понимание онтогенеза иммунной системы может совершить революцию в технологиях трансплантации стволовых клеток и тканевой инженерии, необходимых для иммунотерапии и регенеративной медицины в ближайшем будущем.
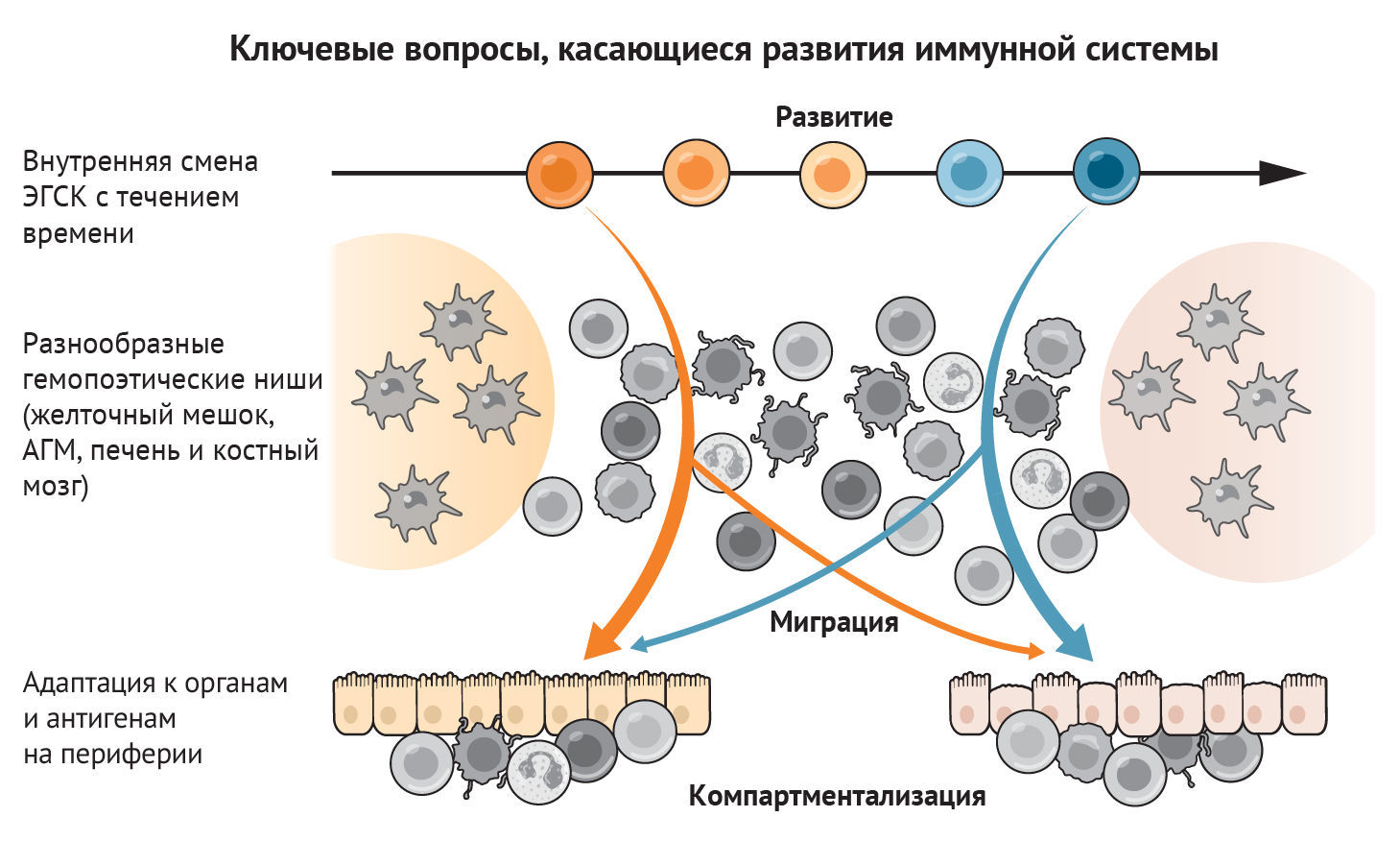
Рисунок 3 | Ключевые вопросы, которые необходимо рассмотреть в будущих исследованиях развития иммунной системы
Диаграмма изображает соответствующие вопросы, касающиеся развития иммунной системы. Как ЭГСК изменяют свой потенциал на протяжении всего развития иммунной системы человека? Чем отличаются различные гемопоэтические ниши друг от друга? Что определяет миграцию иммунных клеток в органы-мишени и как они адаптируются к новой тканевой среде? Методы профилирования отдельных клеток и пространственного профилирования теперь дают ответы на эти вопросы, оценивая иммунную систему в целом и выявляя возникающие свойства клеточного коллектива.
Телеграм: t.me/ainewsline
Источник: medach.pro