Гены и безумие: генетическое тестирование в психиатрии
МЕНЮ
Главная страница
Поиск
Регистрация на сайте
Помощь проекту
Архив новостей
ТЕМЫ
Новости ИИ
Городские сумасшедшие
ИИ в медицине
ИИ проекты
Искусственные нейросети
Искусственный интеллект
Слежка за людьми
Угроза ИИ
ИИ теория
Компьютерные науки
Машинное обуч. (Ошибки)
Машинное обучение
Машинный перевод
Нейронные сети начинающим
Психология ИИ
Реализация ИИ
Реализация нейросетей
Создание беспилотных авто
Трезво про ИИ
Философия ИИ
Генетические алгоритмы
Капсульные нейросети
Основы нейронных сетей
Промпты. Генеративные запросы
Распознавание лиц
Распознавание образов
Распознавание речи
Творчество ИИ
Техническое зрение
Чат-боты
Авторизация
2017-08-26 09:00

Статья на конкурс «био/мол/текст»: Психиатрия на протяжении долгих лет была в стороне от всех основных отраслей медицины. Пока травматологи делали рентгеновские снимки, а терапевты изучали анализы крови, психиатры просто беседовали со своими пациентами и наблюдали за ними. Теперь на помощь психиатрам приходит генетика с ее современными технологиями.
Психиатрии всегда недоставало объективности. Несколько десятилетий назад пациенту могли сделать электроэнцефалографию или пневмовентрикулографию для исключения неврологического расстройства. А если оно подтверждалось, то пациент переходил в руки нейрохирургов или неврологов. Психиатры продолжали работать с теми пациентами, у кого ничего существенного обнаружить не удалось.
С увеличением и усложнением арсенала медицинских исследований психиатрия вроде бы стала заявлять свои права на применение их на регулярной основе, но на деле это не так. Например, мы знаем, что прогрессирование болезни Альцгеймера [1] сопровождается снижением объема гиппокампов — отделов мозга, связанных с памятью [2]. Также известно, что лечение противодементными препаратами может замедлить потерю гиппокампального вещества [3]. Возникает вопрос: как часто пациенту с деменцией делают МРТ головного мозга с подсчетом объема гиппокампов? Ответ лежит на поверхности: практически никогда.
Психические заболевания не берутся на пустом месте. Часто можно выделить провоцирующий социальный фактор в развитии расстройства, но не надо забывать и о биологических факторах. У каждого из нас есть гены, на основе которых строится сложная жизнь наших клеток, в том числе и нейронов. Для того чтобы понять насколько приложимым к реальности может быть генетическое тестирование в психиатрии, необходимо оценить его эффективность и полезность до внедрения в широкую практику. Нам нужно получить ответы на несколько вопросов. Их примерный список может выглядеть так:
- Влияют ли генетические факторы на развитие психических расстройств? Психические расстройства — это большая группа заболеваний, в которой собраны аффективные патологии (депрессия, биполярное аффективное расстройство [БАР], тревожные расстройства), болезни с психотической симптоматикой (шизофрения, состояния спутанности) и нарушения когнитивных функций (умственная отсталость, деменция). Очевидно, что для каждой болезни генетический вклад будет различаться. По этой причине необходимо понять, при каких патологиях он будет максимальным.
- Могут ли эти факторы наследоваться, то есть переходить из поколения в поколение? При помощи генетических исследований мы сможем понять происхождение генетических нарушений при психических расстройствах. Передались ли они от родителей, бабушек и дедушек? Или наблюдаемые изменения возникли у самого пациента (мутации de novo)? Только обширные фундаментальные исследования помогут нам найти ответы на эти вопросы.
- Можно ли выделить конкретный ген или группу генов, которые оказывают заметное влияние на развитие патологии? Поиски ученых приводят к разным результатам. Они могут найти конкретный ген, отвечающий за развитие болезни, а могут обнаружить несколько генов, влияющих на саму болезнь или отдельные симптомы.
- Можем ли мы найти какие-то генетические факторы, которые определяют действие нейролептиков, антидепрессантов и других препаратов при психических расстройствах?Фармакогенетическое тестирование — это определение генетических факторов, связанных с особенностями метаболизма препарата, развитием побочных эффектов при его приеме. Фармакогенетическое тестирование может быть полезно для прогнозирования побочных эффектов и реакции пациента на препарат.
- Разумно ли проводить генетическое тестирование при психических расстройствах с точки зрения этики? Полученные учеными данные могут быть интересными, а сам способ их получения чрезвычайно увлекателен, но нам важно оценить полезность и применимость этой информации. Мы не можем проводить исследования только ради знаний; нам важно, чтобы они были экономически эффективны и не наносили вред пациенту и его семье.
Список можно дополнять в зависимости от обстоятельств, но общий вектор размышлений ясен. Предлагаемое исследование должно быть информативным, а его применение должно быть обоснованным с экономической точки зрения и морально приемлемым. Если нам удастся совместить эти факторы вместе, то генетическое тестирование при психических расстройствах будет иметь смысл.
Происхождение ненормальности
Фундаментальные генетические исследования при психических расстройствах могут принести значительную пользу. Молекулярные методы помогут в классификации психических расстройств, в уточнении их взаимоотношений так же, как они оказались полезны при определении и уточнении степени родства у растений, животных и микроорганизмов. Стоимость генетических исследований постепенно снижается [4], растет их доступность для рядового пользователя и системы здравоохранения в целом (рис. 1). Это означает, что обширные генетические исследования будут все больше и больше входить в повседневную практику исследователей и врачей.
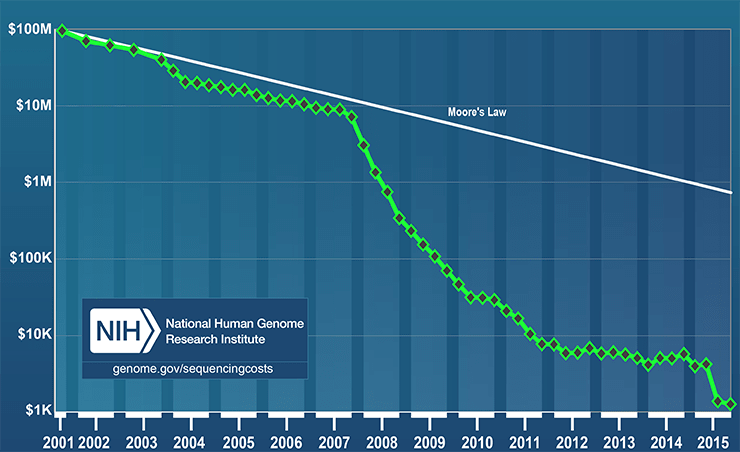
Рисунок 1. Стоимость исследований генома за последние 15 лет значительно снизилась, опередив даже темпы закона Мура.
Диагностика психических расстройств построена на жалобах пациента и результатах осмотра, а не на данных инструментальных исследований. Сейчас в США реализуется проект RDoC (Research Domain Criteria), который направлен на выявление связей между конкретными генетическими вариантами и особенностями функционирования нормального мозга и мозга, затронутого психическим расстройством [5]. Накопление данных по этому проекту может привести к изменению классификации психических расстройств, подходов к их диагностике и лечению.
Сейчас методы генетического тестирования при психических расстройствах, в основном, ограничены поиском хромосомных нарушений (как, например, синдром Дауна) или определением моногенных заболеваний (как, например, ганглиозидоз) (рис. 2).
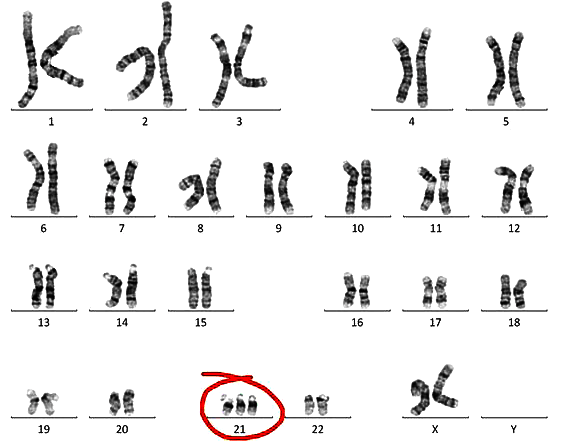
Рисунок 2. Кариотип пациента с синдромом Дауна. Красным обведена дополнительная 21-я хромосома (трисомия по 21-й хромосоме).
сайт pinterest.com
Эти нарушения в структуре ДНК хорошо известны уже десятилетия, и их выявление вошло в привычную медицинскую практику. Проблема психических расстройств заключается в том, что для подавляющего большинства из них нельзя найти конкретный ген, отвечающий за развитие болезни. Психические расстройства — это полигенные заболевания, развитие которых связано с нарушением функции сразу нескольких генов, а также изменениями в сети их взаимодействия. Кроме того, значительная часть случаев заболевания, например, при шизофрении, связана с возникновением мутаций de novo, которые не так уж легко определить [6].
Это приводит к тому, что в сфере генетических исследований появляются новые методы, позволяющие по-новому взглянуть на этот компонент патогенеза [7]:
- Секвенирование экзома (whole exome sequencing) — метод, направленный на исследование той части ДНК, которая кодирует белки. Поскольку на кодирование белков уходит всего 1% всей последовательности ядерной ДНК, этот подход оказывается быстрее и дешевле, чем полногеномное секвенирование.
- Полногеномное секвенирование (whole genome sequencing) изучает не только кодирующую последовательность ядерной ДНК, но и промоторные области, энхансеры, а также митохондриальную ДНК. Этот метод дает огромное количество информации, но ее полезность в каждом конкретном случае оценивается по-разному.
- Секвенирование РНК (RNA-seq) оценивает структуру матричной РНК, которая не является прямой калькой с кодирующей ДНК. В этом преимущество метода: он способен оценить не саму генетическую последовательность, а то, как она воплощается в ходе работы клетки.
В дополнение к этим методам можно исследовать белки, функционирующие внутри нервных клеток, и их взаимодействие. Анализ транскриптома перспективен для изучения генетики психических расстройств. Транскриптом — это совокупность всех РНК, которые производятся в клетке. Благодаря их изучению мы узнаем, какие белки, в каких вариантах и в каком количестве производятся клеткой. Альтернативный сплайсинг происходит в мозге чаще, чем в других органах [8], поэтому сама последовательность ДНК не способна дать нам достаточно информации о том, какие белки синтезируются на ее основе.
В свою очередь сумма генетических нарушений может дать больше, чем каждое из них по отдельности. Уже известны такие сетевые взаимодействия при шизофрении [9] и болезни Альцгеймера с поздним началом [10]. В обширном исследовании 2014-го года обнаружили около 4000 генов, связанных с возникновением расстройств аутистического спектра, синдрома дефицита внимания и гиперактивности (СДВГ), шизофрении и X-сцепленных нарушений интеллектуального развития [11]. Из ряда этих генов выделили 435 наиболее значимых, которые содержали в общей сложности 789 несинонимичных однонуклеотидных замен (SNP). Как показал дальнейший анализ, обнаруженные генетические варианты могли повлиять на ряд важных процессов внутри нервной клетки (рис. 3). Подобные «перекрытия» были обнаружены и в других исследованиях. Например, в развитии пограничного расстройства личности и биполярного аффективного расстройства вовлечен ряд одинаковых генов, например DPYD и PKP4 [12]. Кроме того, при расчете полигенного риска развития некоторых психических расстройств обнаружили их генетическую близость (рис. 4).
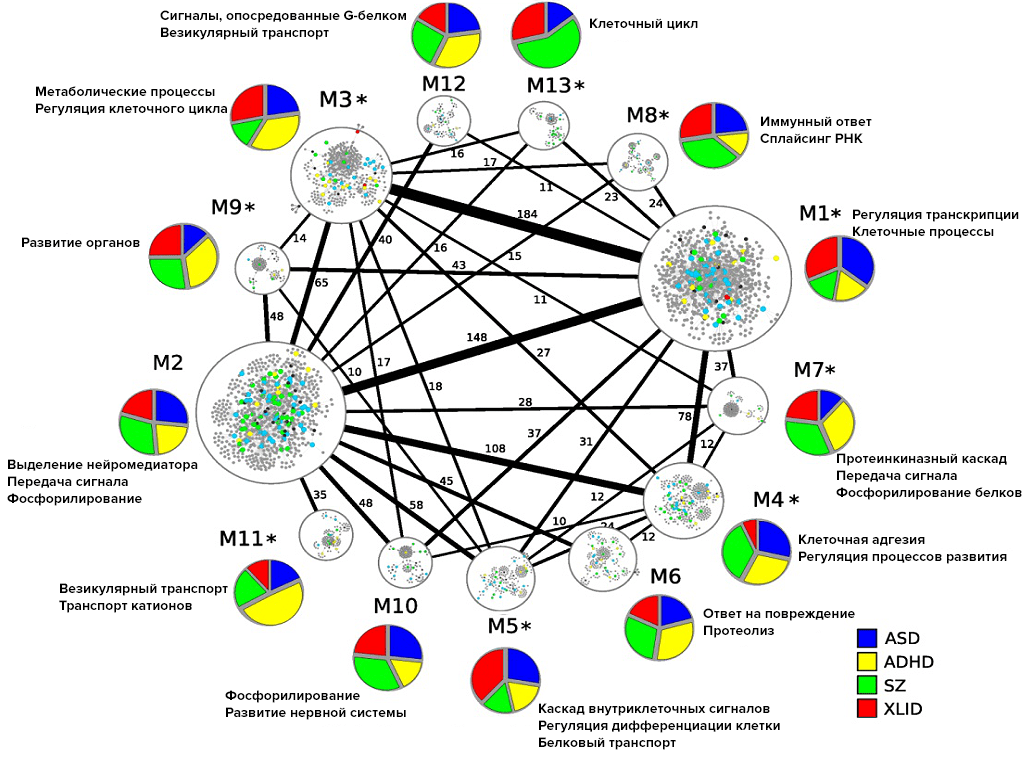
Рисунок 3. Самые разные психические расстройства имеют общие молекулярные основы на уровне белков. Представлены 13 модулей протеинов, вовлеченных в ключевые процессы внутри нейронов. Модули со значительными различиями в частоте первичных генов-кандидатов обозначаются звездочкой. Линии с числами — взаимодействия белков между модулями. Условные обозначения: ASD — расстройства аутистического спектра, ADHD — синдром дефицита внимания и гиперактивности, SZ — шизофрения, XLID — X-сцепленные нарушения интеллектуального развития.
Чтобы увидеть рисунок в полном размере, нажмите на него.
[11], рисунок адаптирован
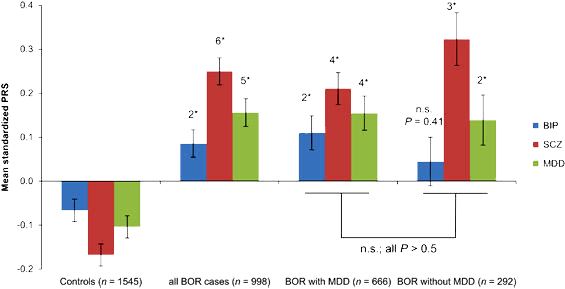
Рисунок 4. При расчете полигенного риска биполярного аффективного расстройства, шизофрении и депрессии обнаружено, что часть генов, ответственных за развитие одной болезни, вовлечена в патогенез других психических расстройств. Условные обозначения: Mean standardized PRS — средняя стандартизованная оценка полигенного риска, BOR — пограничное расстройство личности, BIP — биполярное аффективное расстройство, SCZ — шизофрения, MDD — депрессия.
Отход от поиска конкретных генов приводит к поиску связи между эндофенотипами при шизофрении и изменениями в обширных областях генома [13]. Эндофенотип — это совокупность поведенческих или физиологических признаков, которая является устойчивой и стабильно связана с конкретными изменениями в генетических данных. При этом сами признаки не достигают уровня симптома. Скорее всего, к ним подходит термин «особенность». К эндофенотипам, например, ученые относят нарушение распознавания эмоций и проблемы с тем, как пациент управляет своими движениями. Проблемы с распознаванием эмоций оказались связаны с изменениями на участке хромосомы 1p36, где находится ген, кодирующий серотониновый рецептор 6-го типа. Этот рецептор является мишенью для типичных и атипичных антипсихотиков — препаратов, которые показывают высокую эффективность при лечении шизофрении.
В целом, ситуация с генетическими исследованиями в происхождении психиатрической патологии неутешительна. Слишком много генов влияют на развитие психических расстройств. При этом они оказывают слишком слабые эффекты, требующие новых математических методов для их анализа. Слишком сложные исследования требуются для определения этих слабых связей: они пока малодоступны в широкой практике.
Проверка совместимости
Генетические исследования при психических расстройствах не ограничиваются только поиском причин болезни и их различий. Сейчас все большую популярность приобретает фармакогенетическое тестирование — обнаружение особенностей ферментов, которые задействованы в метаболизме лекарственных средств. В нашем организме есть удивительные труженики — семейство ферментов под названием «цитохром p450». Это семейство включает более 50 ферментов, 6 из которых вовлечены в метаболизм около 90% всех медицинских препаратов [14]. Вот эти ударники метаболического фронта: CYP1A2, CYP2C9, CYP2C19, CYP2D6, CYP3A4 и CYP3A5. Для метаболизма психотропных лекарственных препаратов большое значение имеют CYP2C19 и CYP2D6.
Так, например, 85% антидепрессантов и 40% нейролептиков метаболизирует фермент CYP2D6 [15]. Это находит свое отражение в частоте развития специфических побочных эффектов при использовании психотропных препаратов. Пациенты с высокой активностью CYP2D6, получающие терапию нейролептиками, больше предрасположены к развитию поздней (тардивной) дискинезии, чем те, у кого этот фермент работает менее активно [16]. Поздняя дискинезия представляет собой специфический синдром, вызванный длительным приемом нейролептиков и сохраняющийся после их отмены. При его развитии у пациента появляются насильственные, повторяющиеся движения языка и губ. При тяжелых формах вовлекаются другие группы мышц: у пациента возникают насильственные движения туловища, конечностей. Эти проблемы могут сочетаться с неусидчивостью, тремором и лекарственным паркинсонизмом. Коррекция поздней дискинезии при помощи лекарственных средств — это сложная задача. По этой причине обычно прикладываются усилия по ее предотвращению. Есть данные, которые указывают, что недостаточная активность CYP2D6 может привести к злокачественному нейролептическому синдрому [17]. После приема нейролептиков пациент начинает жаловаться на подъем температуры. У него фиксируется выраженное повышение тонуса мышц, выраженные изменения частоты пульса и артериального давления, а также нарушения сознания различной степени. Это одно из тех редких состояний в психиатрии, которое само по себе может привести к смерти пациента.
Существующие фармакогенетические данные в психиатрии связаны с работой ферментов CYP2C19 и CYP2D6 [18]. Генетическое тестирование может определить скорость работы ферментов в зависимости от того, какая аллель гена представлена у человека и в каком количестве копий. К функциональным вариантам CYP2D6 относятся варианты CYP2D6*1, CYP2D6*2 в любых сочетаниях с другими аллелями. Если этот ген имеет дополнительные копии, то фермент работает слишком активно, что переводит его обладателя в группу «ультрабыстрых» метаболизаторов. «Промежуточные» и «медленные» метаболизаторы по CYP2D6 могут иметь повышенный риск развития побочных эффектов, а значит, требуют меньших доз препаратов при лечении психических расстройств. По активности фермента CYP2C19 людей также можно разделить на «ультрабыстрых», «экстенсивных», «промежуточных» и «медленных» метаболизаторов. Распространенность различных аллелей меняется в зависимости от расы, к которой принадлежит пациент.
Ферменты CYP2C19 и CYP2D6 играют ключевую роль в метаболизме трициклических антидепрессантов, среди которых необходимо упомянуть амитриптилин. Его широко используют психиатры, неврологи и терапевты при самых различных заболеваниях. В ходе метаболизма амитриптилин претерпевает трансформации, приводящие к изменению его влияния на психическое состояние (рис. 5) [18]. Амитриптилин как третичный амин оказывает выраженное воздействие на серотониновую систему. Благодаря воздействию CYP2C19, он превращается в нортриптилин, который активно вмешивается в работу норадреналиновой передачи. Чем активнее работает фермент, тем слабее «серотониновый» компонент воздействия амитриптилина и тем сильнее норадреналиновый. Так как CYP2D6 вовлечен в метаболизм трициклических антидепрессантов, его активность влияет на способность препаратов воздействовать на состояние пациента. У «ультрабыстрых» метаболизаторов по CYP2D6 терапию рекомендуют начинать не с этого класса препаратов. Если пациент с такими особенностями метаболизма получает терапию трицикликами, то необходимо регулярно оценивать концентрацию препарата в плазме. Для «медленных» метаболизаторов рекомендации такие же. Если им приходится принимать трициклические антидепрессанты, то начальная доза должна составлять 50% от рекомендованной стартовой. Схожие рекомендации существуют и для CYP2C19 [18]. При этом не надо думать, что генетическое тестирование обсуждаемых ферментов — это какая-то экзотика. В 2005 году FDA одобрила систему AmpliChip CYP450, которая дает данные по генетике этих ферментов. Отдельные исследования генов CYP2C19 и CYP2D6 доступны и в нашей стране.
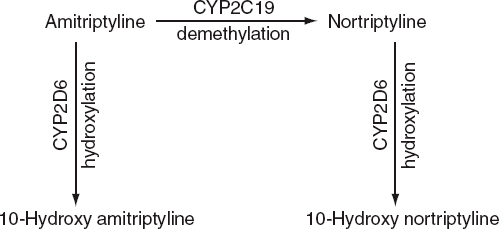
Рисунок 5. В организме человека амитриптилин при помощи фермента CYP2C19 превращается в нортриптилин, активный метаболит амитриптилина. CYP2D6 участвует в превращении обеих молекул в неактивную форму.
Еще одним примером уже существующего фармакогенетического тестирования, направленного на предотвращение редких, но опасных побочных эффектов, является скрининг маркера HLA-B*1502 у лиц азиатского происхождения. При терапии карбамазепином у пациентов, имеющих этот ген, повышается риск развития синдрома Стивенса—Джонсона, потенциально смертельного поражения кожи, при котором клетки эпидермиса отделяются от дермы [19]. FDA рекомендует проводить определение маркера HLA-B*1502 перед началом терапии карбамазепином.
Многие знания — многие печали?
Каждый раз, когда речь заходит о внедрении и использовании диагностического метода в медицинскую практику, необходимо оценить его полезность. Если мы начнем проводить генетические тесты пациентам с психическими расстройствами, будет ли это полезно для них? Получим ли мы какую-то значимую информацию для диагностики и лечения этой группы заболеваний?
На текущем этапе развития генетики психических расстройств польза от них сомнительна. Слишком много неопределенных и плохо применимых на практике результатов дают исследования даже с большой выборкой. Главной причиной этого является кардинальное отличие психических расстройств от моногенных заболеваний. В классическом случае моногенного заболевания (например, болезни Гентингтона) достаточно проанализировать структуру одного гена, чтобы понять, есть у пациента это расстройство или нет. С такой же определенностью это будет работать для прогнозирования развития болезни Гентингтона у потенциального носителя гена. Можно вспомнить Тринадцатую из сериала «Доктор Хаус», которая одним анализом выяснила, разовьется у нее болезнь Гентингтона или нет [20].
Психические расстройства имеют другую генетическую основу. Это полигенные заболевания, развитие которых связано с изменением работы многих генов одновременно. Выявление каждого из этих генов не принесет важной диагностической информации для врача, по крайней мере, на текущем этапе развития этой области знаний. Также мало смысла сейчас в прогнозировании риска развития психического расстройства на основе генетических исследований у каждого человека и родственников уже известных пациентов. В развитии психических расстройств большую роль играют средовые факторы — социально-экономическое положение, серьезные потрясения в жизни, место проживания человека. Неопределенная информация, которую получит человек, не страдающий психическим расстройством, приведет к повышению тревоги у него за свое здоровье, а это излишнее беспокойство может спровоцировать возникновение у него болезни («Я беспокоился, что сойду с ума, и в итоге сошел с ума»). Другой стороной выявления у человека подобных генетических рисков является негативное отношение к нему со стороны окружающих («У него есть гены шизофрении, а значит, он в любой момент может стать шизофреником»). Это будет существенно осложнять жизнь человека. Хотя риск сам по себе может быть незначительным, все слова и решения человека могут быть восприняты через призму его потенциального безумия. Человек с просчитанным риском психического расстройства может быть признан больным еще без самой болезни. Польза тут, конечно, сомнительна.
Подобная проблема хорошо иллюстрируется исследованиями гена 5-HTTLPR (серотониновый транспортер), который часто связывают с риском антисоциального поведения (агрессия, преступления против собственности). Короткая версия гена с небольшим количеством повторов в его структуре делает человека уязвимым к внешним проявлениям угрожающих ситуаций и провоцирует повышенную активность гипоталамо-гипофизарно-надпочечниковой системы [21]. В итоге подросток-обладатель короткой версии гена 5-HTTLPR будет с большей вероятностью демонстрировать антисоциальное поведение, чем тот, у кого есть длинный вариант этого гена. Пока все ясно: возьмем всех подростков, протестируем их на этот ген. Затем сформируем группу риска и будем вести за ней пристальное наблюдение, чтобы предотвращать преступления и попадание этих молодых людей в тюрьму. Как говорится, было гладко на бумаге да забыли про овраги. «Оврагом» в этом случае выступают факторы среды, в частности, социально-экономические условия, в которых растет подросток. Если мы говорим о неблагополучных районах, то в них преобладающие влияние на антисоциальное поведение оказывают экономические и социальные факторы (безработица, уровень образования) [22]. Значит, для предотвращения преступлений необходимы интервенции на уровне всей местности, меры, улучшающие социальный климат в целом. Влияние вариантов гена 5-HTTLPR становится заметным при благополучных социально-экономических условиях. Получается, что «генетических» хулиганов надо искать не в трущобах и гетто, а среди представителей среднего класса и обеспеченных горожан, что несколько обескураживает.
Развитие генетических исследований в сфере психических расстройств будет продолжаться. Благодаря проведенным исследованиям, у нас есть данные по фармакогенетике, которые позволяют с умом подобрать лечение, чтобы избежать побочных эффектов и достичь хорошего результата терапии. Расчет рисков развития болезни и диагностика психических расстройств пока остаются сложной и недостижимой на практике задачей. Будем надеяться, что со временем это изменится.
Литература
- На руинах памяти: настоящее и будущее болезни Альцгеймера;
- Jack C.R. Jr., Petersen R.C., Xu Y., O’Brien P.C., Smith G.E., Ivnik R.J. et al. (2000). Rates of hippocampal atrophy correlate with change in clinical status in aging and AD. Neurology. 55, 484–89;
- Mamoru Hashimoto, Hiroaki Kazui, Keiji Matsumoto, Yoko Nakano, Minoru Yasuda, Etsuro Mori. (2005). Does Donepezil Treatment Slow the Progression of Hippocampal Atrophy in Patients With Alzheimer’s Disease?. AJP. 162, 676-682;
- DNA sequencing costs: data. (2016). National Human Genome Research Institute;
- Research Domain Criteria (RDoC). National Institute of Mental Health;
- Hui Liu, Simon C. Heath, Christina Sobin, J. Louw Roos, Brandi L. Galke, et. al.. (2002). Genetic variation at the 22q11PRODH2/DGCR6locus presents an unusual pattern and increases susceptibility to schizophrenia. PNAS. 99, 3717-3722;
- U Demkow, T Wola?czyk. (2017). Genetic tests in major psychiatric disorders—integrating molecular medicine with clinical psychiatry—why is it so difficult?. Transl Psychiatry. 7, e1151;
- Qun Pan, Ofer Shai, Leo J Lee, Brendan J Frey, Benjamin J Blencowe. (2008). Deep surveying of alternative splicing complexity in the human transcriptome by high-throughput sequencing. Nat Genet. 40, 1413-1415;
- C Chen, L Cheng, K Grennan, F Pibiri, C Zhang, et. al.. (2013). Two gene co-expression modules differentiate psychotics and controls. Mol Psychiatry. 18, 1308-1314;
- Bin Zhang, Chris Gaiteri, Liviu-Gabriel Bodea, Zhi Wang, Joshua McElwee, et. al.. (2013). Integrated Systems Approach Identifies Genetic Nodes and Networks in Late-Onset Alzheimer’s Disease. Cell. 153, 707-720;
- A S Cristino, S M Williams, Z Hawi, J-Y An, M A Bellgrove, et. al.. (2014). Neurodevelopmental and neuropsychiatric disorders represent an interconnected molecular system. Mol Psychiatry. 19, 294-301;
- S H Witt, F Streit, M Jungkunz, J Frank, S Awasthi, et. al.. (2017). Genome-wide association study of borderline personality disorder reveals genetic overlap with bipolar disorder, major depression and schizophrenia. Transl Psychiatry. 7, e1155;
- Tiffany A. Greenwood, Neal R. Swerdlow, Raquel E. Gur, Kristin S. Cadenhead, Monica E. Calkins, et. al.. (2013). Genome-Wide Linkage Analyses of 12 Endophenotypes for Schizophrenia From the Consortium on the Genetics of Schizophrenia. AJP. 170, 521-532;
- Lynch T. and Price A. (2007). The effect of cytochrome P450 metabolism on drug response, interactions, and adverse effects. Am. Fam. Physician. 76, 391–396;
- Needham D., Teed N., Pippins J. (2011). CYP2D6 and CYP2C19 genetic testing for psychiatric drug response. Personalized Medicine Portal;
- Maju M Koola, Evangelia M Tsapakis, Padraig Wright, Shubulade Smith, Robert W Kerwin (RIP), et. al.. (2014). Association of tardive dyskinesia with variation in CYP2D6: Is there a role for active metabolites?. J Psychopharmacol. 28, 665-670;
- Agnieszka Butwicka, Szyma?ska Krystyna, W?odzimierz Retka, Tomasz Wola?czyk. (2014). Neuroleptic malignant syndrome in an adolescent with CYP2D6 deficiency. Eur J Pediatr. 173, 1639-1642;
- J K Hicks, J J Swen, C F Thorn, K Sangkuhl, E D Kharasch, et. al.. (2013). Clinical Pharmacogenetics Implementation Consortium Guideline for CYP2D6 and CYP2C19 Genotypes and Dosing of Tricyclic Antidepressants. Clin Pharmacol Ther. 93, 402-408;
- P Brent Ferrell, Howard L McLeod. (2008). Carbamazepine,HLA-B*1502and risk of Stevens–Johnson syndrome and toxic epidermal necrolysis: US FDA recommendations. Pharmacogenomics. 9, 1543-1546;
- Как спасти Тринадцатую? (Перспективы лечения болезни Хантингтона);
- Jorim J. Tielbeek, Richard Karlsson Linn?r, Koko Beers, Danielle Posthuma, Arne Popma, Tinca J. C. Polderman. (2016). Meta-analysis of the serotonin transporter promoter variant (5-HTTLPR) in relation to adverse environment and antisocial behavior. Am. J. Med. Genet.. 171, 748-760;
- Catherine Tuvblad, Martin Grann, Paul Lichtenstein. (2006). Heritability for adolescent antisocial behavior differs with socioeconomic status: gene-environment interaction. J Child Psychol & Psychiat. 47, 734-743.
Телеграм: t.me/ainewsline
Источник: biomolecula.ru