Клеточный атлас показывает ландшафт ранней беременности
МЕНЮ
Искусственный интеллект
Поиск
Регистрация на сайте
Помощь проекту
ТЕМЫ
Новости ИИ
Голосовой помощник
Городские сумасшедшие
ИИ в медицине
ИИ проекты
Искусственные нейросети
Слежка за людьми
Угроза ИИ
Компьютерные науки
Машинное обуч. (Ошибки)
Машинное обучение
Машинный перевод
Реализация ИИ
Реализация нейросетей
Создание беспилотных авто
Трезво про ИИ
Философия ИИ
Генетические алгоритмы
Капсульные нейросети
Основы нейронных сетей
Распознавание лиц
Распознавание образов
Распознавание речи
Техническое зрение
Чат-боты
Авторизация
2018-11-24 17:30
Исследователей давно интересовал «иммунологический парадокс» беременности: как организм матери переносит ребёнка с ДНК отца. Для того чтобы найти ответы, Розер Венто-Тормо (Roser Vento-Tormo) из Института Сенгера с коллегами провели секвенирование РНК одиночных клеток (scRNAseq), выделенных из плаценты и децидуальной ткани, сопоставив данные с клетками крови матери. Для анализа очень больших наборов данных команда создала вычислительную платформу CellPhoneDB, которая осуществляет статистическое прогнозирование пар рецептор-лиганд между различными типами клеток. Составленный ими молекулярный атлас является впечатляющим ресурсом для будущих исследований беременности и её осложнений, таких как различные инфекции.
Секвенирование РНК тысяч одиночных клеток, расположенных на стыке матери и плода в начале беременности, показывает замечательную сложность в типах клеток и регуляторных сетях, которые поддерживают размножение.
Ученые долго ломали голову над иммунологический парадокс беременности1: как мать терпеть плода — иностранное юридическое лицо, которое несет в себе определенную отца ДНК? В статье в природе, Венто-Тормо и соавт.Два исследуйте эту загадку. Авторы выполняли одноклеточное секвенирование РНК (скрнасек) клеток, выделенных из плаценты и децидуа (слизистой оболочки беременной матки), и из соответствующей материнской крови для сравнения. Они определили ряд типов клеток, уникальных для этого материнско-фетального интерфейса, и предположили существование большой сети потенциальных взаимодействий между ними, которые будут способствовать иммунологической толерантности и лелеять рост плода. Авторский молекулярный атлас предоставляет впечатляющий ресурс для будущих исследований беременности и ее осложнений.
Ранний эмбрион развивается в структуру, называемую бластоцист, которая имплантируется в слизистую оболочку матки. Имплантация запускает развитие плаценты из плодных оболочек. Плацента питает плод через пуповину3. Аномальное развитие плаценты может привести к нескольким осложнениям беременности, включая преэклампсию, ограничение роста плода и мертворождение. Необходимо лучшее понимание развития плаценты человека, но для этого процесса нет хорошей модели животного-он должен изучаться у женщин.
Венто-Тормо и соавт. были взяты плацентарные, децидуальные и кровяные пробы от беременностей, которые по выбору прерывались в период между 6 и 14 неделями беременности. Анализ scRNAseq позволил провести различие между клетками материнского и фетального происхождения, поскольку последние включают в себя последовательности РНК, отсутствующие у матери. Это ясно показало, что клетки плода мигрировали в материнскую децидуа (Рис. 1), и что небольшое подмножество материнских иммунных клеток, называемых макрофагами, было расположено в плаценте.
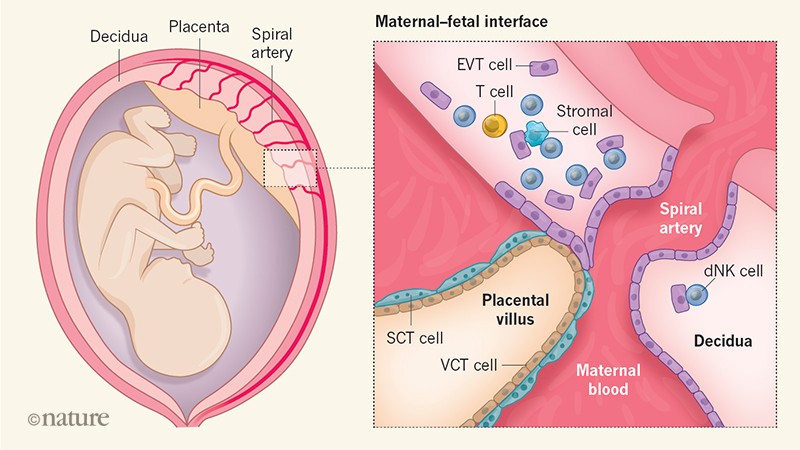
Рисунок 1 / атлас клеток на интерфейсе матери и плода. Во время первого триместра беременности человека, форм взаимодействия между материнской оболочки (оболочки беременной матки) и плода плаценты. Питательные вещества доставляются в плаценту по спиральным артериям матери. Венто-Тормо и соавт.Два секвенировал РНК тысяч одиночных клеток на этом интерфейсе, и использовал данные для того чтобы определить различные типы клетки и предсказать взаимодействия между клетками на основании приемных устройств и молекул лиганда которые они выражают (не показанный). Данные авторов дают информацию о типах клеток плода, полученных из раннего эмбриона: клетки виллозного цитотрофобласта (ДКТ), линии плацентарных структур которых называются ворсинками; клетки синцитиотрофобласта (СКТ), покрывающие поверхность ворсаи экстравилловые клетки трофобласта (EVT), которые выстраивают в линию материнские кровеносные сосуды и смешивают с материнскими клетками в децидуа. Авторы также выявили несколько типов иммунной клетки матери, включая т-клетки и три подмножества децидуальной природной киллерной (dNK) клетки, и три типа стромальной клетки, которые обеспечивают структурную поддержку децидуа.
Эмбрион бластоцист-стадии играет активную роль в собственной судьбе. Клетки из наружного слоя бластоцисты, называемые клетками трофобласта, подвергаются дифференцировке. Венто-Тормо и его коллеги определили факторы транскрипции, участвующие в дифференцировке одного типа клеток трофобласта, клеток ворсистой цитотрофобласта (VCT), либо в клетки синцитиотрофобласта, либо в клетки экстравиллусной трофобласта (EVT) (Рис. 1). Авторы обнаружили, что клетки ДКТ выражают рецепторы, которые способствуют дифференцировке и стимулируются факторами роста, создаваемыми различными клетками плаценты.Клетки ЭВТ вторгаются в децидуа, где они взаимодействуют с материнскими белыми кровяными клетками для того чтобы вызвать ремоделинг узких материнских спиральных артерий в более широкие проводники которые могут отвечать питательные потребностямы превращаясь плода. Авторы показали, что такие инвазивные EVT — клетки производят сигнальный белок, называемый трансформирующим фактором роста ?, который способствует развитию материнских регуляторных T — клеток-подмножества иммунных клеток, называемых T-клетками, которые обуздывают иммунные реакции.
Самый распространенный материнских иммунных клеток в оболочки во время первого триместра беременности являются естественные киллерные (NK) клетки4. Наиболее известен как убийц инфицированных клеток и опухолевых клеток, NK-клетки принимают более мирную роль во время беременности, и выделения растворимых белков, которые способствуют материнской кровеносных сосудов перепланировка3,5. Децидуальные НК (ДНК) клетки и регулируют степень, в которой ЭВТ клетки могут вторгаться в оболочки4. Венто-Тормо и соавт. выделено три подмножества клеток dNK-замечательное открытие, поскольку оно показывает, что клетки dNK превратились в специализированные клетки, которые очень отличаются от клеток NK крови. Данные авторов показывают, что иммунологическая активность каждого подмножества ДНК продиктована их способностью взаимодействовать как с материнскими, так и с фетальными клетками в децидуа, с двойным исходом, способствующим росту плода и сдерживающим иммунным нападением на клетки плода.
Работа исследователей также показывает, что два слоя decidua определяются различными молекулярными профилями и содержат различные дополнения пяти типов клеток: два типа периваскулярной клетки, которые поддерживают материнские кровеносные сосуды, и три типа децидуальной стромальной (dS) клетки, которые обеспечивают тканям структурную поддержку.Клетки ДС выражают интерлеукин-15 протеина, которое необходимо для выживания и пролиферации НК-клетки, и лиганды для 2 инхибиторы приемных устройств на клетках НК, показывая роль клеток ДС в поддерживать выживание клеток НК пока ограничивающ их иммунную функцию.
To analyse their very large data sets, Vento-Tormo et al. created a computational platform, CellPhoneDB, to statistically predict receptor–ligand pairs between the different cell types identified by scRNAseq. The platform is publicly available (CellPhoneDB.org) as a resource for examining gene-expression profiles of single cells and for making inferences about networks of cell–cell communication. The authors have highlighted just a few of the cellular interactions revealed by their analysis. Many more remain, and await interrogation.
Есть врожденные ограничения в изучении размножения человека. В этом случае образцы из беременности на 6-14 неделе беременности рассматривались как эквивалент. Но за это время плод питается двумя различными способами — Во-первых, желез матки, которые питаются в intravillous пространства плаценты, и, позже, по материнской крови, которая проходит непосредственно развивающейся плаценты6. Рассматривая эти два этапа как один из них может скрыть ценную информацию. Кроме того, не были изучены изменения, происходящие на более ранних стадиях развития эмбриона. Очевидно, систематического анализа продольных внутриутробное развитие человека не представляется возможным, из-за этических вопросов.
Основным препятствием для понимания человеческого развития является отсутствие репрезентативных моделей животных. Венто-Тормо и соавт. теперь обеспечьте человеческую молекулярную ссылку, против которой беременность у животных может быть проанализирована, чтобы найти признаки, которые делятся с людьми. Кроме того, с помощью этого ресурса можно оценить данные, полученные от женщин с осложнениями беременности. Это может привести к выявлению биомаркеров распространенных осложнений беременности.
Путем картирования клетчатой и молекулярной местности первого триместра беременности человека, настоящее исследование освещает как материнско-фетальный интерфейс мирная и терпимая окружающая среда в которой иммунологическая реактивность смочена. В такой среде, материнские и фетальные клетки сотрудничают для того чтобы отрегулировать нашествие trophoblast, remodel материнское vasculature и обеспечить достаточное питание для плода. Однако такая иммунологическая толерантность может стоить дорого. Например, известная уязвимость к определенным инфекциям7, как цитомегаловирус, вирус Зика и маляри-причиняя паразиты, во время этого времени в беременности смог быть из-за задержанной иммунной реактивности. Данные Vento-Tormo и коллег обеспечивают мощную основу для оценки условий ранней беременности во время таких разрушительных инфекций.
Источник: www.nature.com